题目内容
【题目】短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2 为红棕色气体,Y的单质既能与强酸又能与强碱反应,W、Z 最外层电子数之和是X最外层电子数的2 倍。下列说法中错误的是
A. Y 与X、Y与Z均形成离子化合物
B. 对应简单离子的半径:W>X>Y
C. Z 对应的最高价含氧酸是一元强酸
D. ZX2 是一种消毒能力强于氯气且更加安全的自来水消毒剂
【答案】A
【解析】短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2 为红棕色气体NO2,则W为氮元素、X为氧元素;Y的单质既能与强酸又能与强碱反应,则Y为铝元素,W、Z 最外层电子数之和是X最外层电子数的2 倍,则Z的最外层电子 数为![]() ,且Z的原子序数大于铝,则Z为氯元素。A. Y 与X形成氧化铝属于离子化合物,Y与Z形成氯化铝属于共价化合物,选项A错误;B. 具有相同电子层结构的离子核电荷数越大半径越小,故对应简单离子的半径:N3->O2->Al3+,选项B正确;C. Z 对应的最高价含氧酸HClO4是一元强酸,选项C正确;D. ZX2 为二氧化氯,是一种消毒能力强于氯气且更加安全的自来水消毒剂,选项D正确。答案选A。
,且Z的原子序数大于铝,则Z为氯元素。A. Y 与X形成氧化铝属于离子化合物,Y与Z形成氯化铝属于共价化合物,选项A错误;B. 具有相同电子层结构的离子核电荷数越大半径越小,故对应简单离子的半径:N3->O2->Al3+,选项B正确;C. Z 对应的最高价含氧酸HClO4是一元强酸,选项C正确;D. ZX2 为二氧化氯,是一种消毒能力强于氯气且更加安全的自来水消毒剂,选项D正确。答案选A。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案【题目】现有四组分散系:①汽油和水形成的乳浊液;②含有泥沙的食盐水;③溶有碘(I2)的酒精溶液;④乙二醇和丙三醇的混合溶液(乙二醇和丙三醇的部分物理性质见下表)。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )
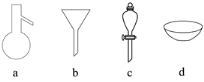
A. ①―c―分液 B. ②―b―过滤 C. ③―d―蒸发结晶 D. ④―a―蒸馏
【题目】探究Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O 反应的速率影响因素,设计了以下实验,下列说法正确的是
锥形瓶 | 0.1molLNa2S2O3 溶液/mL | 蒸馏水 | 0.2mol/L H2SO4 溶液 | 反应温度 | 浑浊出现时间/s | 备注 |
1 | 10 | 0 | 10 | 20℃ | 10 | |
2 | 10 | 5 | 5 | 20℃ | 16 | |
3 | 10 | 0 | 10 | 50℃ | 5 | 第10 秒开始浑浊不再增多 |
4 | 10 | 6 | 4 | 50℃ | 8 |
A. 该反应也可通过测SO2的体积变化来表示化学反应速率的快慢
B. 3号瓶用Na2S2O3 来表示速率为0.0lmol/(Ls)
C. 由2号瓶和3号瓶实验结果可得温度越高反应速率越快
D. 由1号瓶和4号瓶实验结果可得温度越高反应速率越快