题目内容
【题目】下列规律与化学反应的能量变化关系最大的是
A.阿伏加德罗定律 B.盖斯定律 C.勒夏特列原理 D.欧姆定律
【答案】B
【解析】
试题A.阿伏加德罗定律反映的是气体的分子数与气体的体积、外界条件的关系的知识,与能量变化关系不是很大,错误;B.盖斯定律表示的是物质发生反应时的能量变化只与物质的存在状态与物质的多少有关,而与反应途径无关,因此表示的是与化学反应的能量变化关系最大的规律,正确;C. 勒夏特列原理表示是可逆化学反应变化的规律,如果改变影响化学平衡的一个条件,化学平衡会向能够减弱这种改变的方向移动,与化学反应的能量变化关系不大,错误;D.欧姆定律是计算电流与电压关系的规律,与能量变化关系不大,错误。

【题目】一氧化碳是一种用途相当广泛的化工基础原料。
⑴.利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
Ni(s)+4CO(g)![]() Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
⑵.在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g);ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)=2CO(g);ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)=SO2(g);ΔH3=-296.0 kJ·mol-1
则2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH4=________。
⑶.工业上一般采用CO与H2反应合成可再生能源甲醇,反应如下:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测
得c(CO)=0.2mol·L-1,则CO的转化率为___________。
合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160。此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
物质 | H2 | CO | CH3OH |
浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
比较此时正、逆反应速率的大小:v正_______v逆 (填“>”、“<”或“=”);若其他条件不变,在T2℃反应10min后达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率:v(CH3OH)=__________;
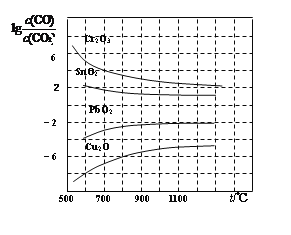
(4)金属氧化物被一氧化碳还原生成金属单质和二氧化碳。下图是四种金属氧化物被一氧化碳还原时lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。800℃时,其中最易被还原的金属氧化物是____(填化学式),该反应的平衡常数数值(K)等于____________。