题目内容
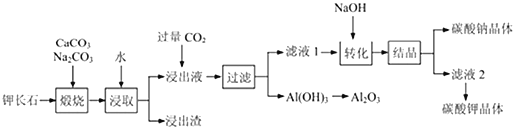
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、C、d.e、f是由这些元素组成的化合物,d为淡黄色的离子化合物,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径:W<X<Y<Z
B. 简单气态氢化物的热稳定性:X>Y
C. 图中物质的转化过程均为氧化还原反应
D. a一定由W、X两种元素组成
【答案】C
【解析】
本题考查无机物的推断,为高频考点,侧重分析与推断能力的考查,把握钠的化合物的性质及相互转化为解答的关键,注意淡黄色固体、原子序数为推断的突破口,难度不大。
短周期元素W、X、Y、Z的原子序数依次递增,a、b、C、d.e、f是由这些元素组成的化合物,d为淡黄色的离子化合物,为过氧化钠,m为元素Y的单质,通常为无色无味的气体,为氧气,则Y为氧,a为烃或烃的含氧衍生物,b、c分别为二氧化碳和水,e、f分别为氢氧化钠和碳酸钠,结合原子序数可知,W为氢,X为碳,Y为氧,Z为钠。A.根据电子层数越多,半径越大,电子层数相同的原子原子序数越大,半径越小分析,四种元素原子半径的大小顺序为W<Y<X<Z,故错误;B.非金属性越强,氢化物越稳定,氧非金属性比碳强,所以稳定性顺序为X<Y,故错误;C.图中涉及的反应都有化合价变化,都为氧化还原反应,故正确;D.a含有碳和氢元素,还可能含有氧元素,故错误。故选C。

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
【题目】如图图象中,纵坐标为沉淀物的物质的悬,横坐标为向溶液中加入反应物的物质的量,则相应的图象序号与(1)﹣(4)对应的是 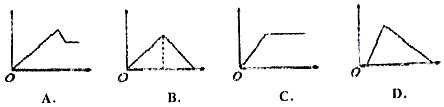
溶液 | 加入物质 | 对应的图象 |
⑴饱和石灰水 | 通过量CO2气体 | |
⑵氯化铝溶液 | 加入过量氨水 | |
⑶MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | |
⑷含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |