题目内容
密闭容器中,发生反应:CO(g) + 2H2(g) CH3OH(g) △H<0,下列说法正确的是
CH3OH(g) △H<0,下列说法正确的是
 CH3OH(g) △H<0,下列说法正确的是
CH3OH(g) △H<0,下列说法正确的是| A.一定温度下,压缩容器体积,则正反应速率加快,逆反应速率减慢 |
| B.若v生成(CH3OH)=v消耗(CO),则该反应达到平衡状态 |
C.升高温度,重新达到平衡时,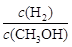 增大 增大 |
| D.使用催化剂,反应的平衡常数增大 |
C
试题分析:A、一定温度下,压缩容器体积,压强增大。则正反应速率加快,逆反应速率也加快,A不正确; B、v生成(CH3OH)=v消耗(CO),根据方程式可知,二者的反应速率之比始终是相等的,因此不能说明该反应达到平衡状态,B不正确;C、正方应是放热反应,升高温度,平衡向逆反应方向移动,重新达到平衡时,
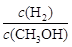 增大,C正确;D、平衡常数只与温度有关系,因此使用催化剂,反应的平衡常数不变,D不正确,答案选C。
增大,C正确;D、平衡常数只与温度有关系,因此使用催化剂,反应的平衡常数不变,D不正确,答案选C。
练习册系列答案
相关题目
 Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是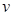 (H2O)=
(H2O)=
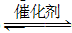 CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH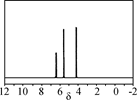
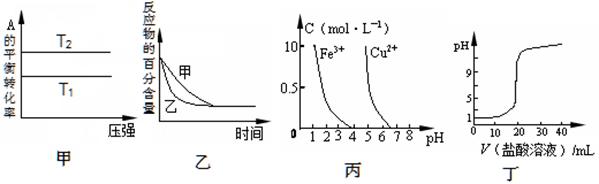
 2C(g)的△H<0
2C(g)的△H<0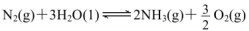
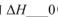 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。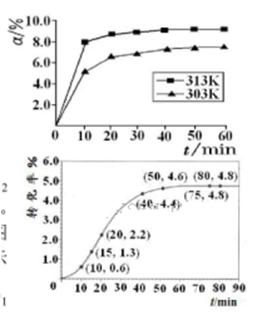
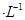 盐酸与0.2 mol
盐酸与0.2 mol (25℃时,NH3.H2O的电离常数
(25℃时,NH3.H2O的电离常数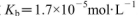 )
)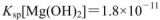 ,
,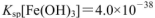 )
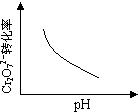
) 2PbCrO4(s)+2H+(aq)△H<0
2PbCrO4(s)+2H+(aq)△H<0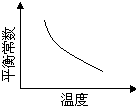
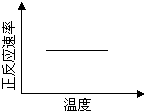
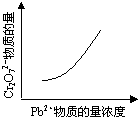
 CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l)  ,该反应在 (填“较高温度”或“较低温度”)下能自发进行。
,该反应在 (填“较高温度”或“较低温度”)下能自发进行。



 物质
物质 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( ) Cl2(l) ],应采取的措施是_______(写出一条即可)。
Cl2(l) ],应采取的措施是_______(写出一条即可)。