题目内容
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是

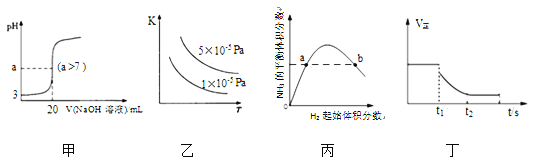
A. 图①表示不同压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
B. 图②表示向10ml0.1mol·L-1Na2CO3和NaHCO3两种溶液中分别滴加0.lnol·L-1HCl溶液时,CO2的体积随盐酸体积的变化,则b表示的是NaHCO3溶液
C. 图③表示体积和pH均相同的HCl、CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示的是HCl溶液
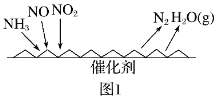
D. 图④表示该反应为放热反应,且催化剂能改变反应的焓变
【答案】B
【解析】
解:A、图①增大压强对可逆反应2A(g)+2B(g)![]() 3C(g) +D(s)平衡正向移动,图①说明乙的压强比甲大,反应物的含量不相等,故A错误;B、碳酸钠溶液中滴入盐酸先生成碳酸氢钠后,继续滴入盐酸开始生成气体。碳酸氢钠溶液中滴入盐酸开始有气体生成,b为碳酸氢钠溶液,故B正确; C、盐酸和醋酸是一元酸,醋酸是弱酸,盐酸是强酸,如果体积和pH均相同,醋酸的浓度大,与金属反应放出的气体多。 a表示的是醋酸。所以C选项是错误的;D. 图④表示该反应为放热反应,催化剂只能降低反应的活化能,不能改变反应的焓变。所以D选项是错误的。本题正确答案:B。
3C(g) +D(s)平衡正向移动,图①说明乙的压强比甲大,反应物的含量不相等,故A错误;B、碳酸钠溶液中滴入盐酸先生成碳酸氢钠后,继续滴入盐酸开始生成气体。碳酸氢钠溶液中滴入盐酸开始有气体生成,b为碳酸氢钠溶液,故B正确; C、盐酸和醋酸是一元酸,醋酸是弱酸,盐酸是强酸,如果体积和pH均相同,醋酸的浓度大,与金属反应放出的气体多。 a表示的是醋酸。所以C选项是错误的;D. 图④表示该反应为放热反应,催化剂只能降低反应的活化能,不能改变反应的焓变。所以D选项是错误的。本题正确答案:B。

 阅读快车系列答案
阅读快车系列答案【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污
泥中Cr(Ⅲ)的处理工艺流程如下:

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1)实验室用18.4 mol·L-1的浓硫酸配制480 mL 2 mol·L-1的硫酸,需量取浓硫酸___mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需____________________________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:
___________________________________________。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O72-转化为__________(填微粒的化学式)
(4)钠离子交换树脂的反应原理为:Mn+ + n NaR = MRn + n Na+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有__________________。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式______________________________。
(6)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 黄 | 白 | 砖红 | 白 |
Ksp | 1.8×10-10 | 8.3×10-17 | 1.2×10-16 | 3.5×10-11 | 1.0×10-12 |
滴定时可选为滴定指示剂的是____(选填编号),滴定终点现象是________________________。
A.NaCl B.K2CrO4 C.KI D.NaCN
【题目】能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO 的燃烧热(△H)分别为-a kJmol-1、-b kJmol-1、-c kJmol-1;
②H2O (l) =H2O(g); △H=+dkJmol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJmol-1。
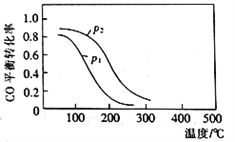
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________ (填“>”“<”或“ = ”)0。
②下列说法正确的是____________ (填标号)。
a.温度越高,该反应的平衡常数越大 b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度 d.图中压强p1<p2
③200℃时,该反应的平衡常数K =_______。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为_________。
(4)有人设计将两根 Pt 丝作电极插入 KOH 溶液中,然后向两极上分别通入乙醇和氧气而 构成燃料电池。则此燃料电池工作时,其电极反应式为:
负极:_____________
正极:_____________