题目内容
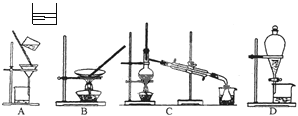
用于分离或提纯物质的方法有:A蒸馏(分馏);B萃取;C过滤;D重结晶;E分液。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号)
(1)淀粉液中含有泥沙 ;
(2)分离四氯化碳与水的混合物 ;
(3)分离汽油和煤油 ;
(4)分离碘水中的碘单质 ;
(5)KNO3晶体中含有少量食盐 。
(1)淀粉液中含有泥沙 ;
(2)分离四氯化碳与水的混合物 ;
(3)分离汽油和煤油 ;
(4)分离碘水中的碘单质 ;
(5)KNO3晶体中含有少量食盐 。
(1)C (2)E (3)A (4)BE (5)D
试题分析:(1)淀粉液中含有泥沙,泥沙不溶解于水,淀粉溶解,故采用过滤法分离。(2)分离四氯化碳与水的混合物它们是互不相溶的液体,可采用分液法分离。(3)分离汽油和煤油 二者互溶且沸点不同,可采用蒸馏方法分离。(4)分离碘水中的碘单质 可以利用碘单质在四氯化碳中的溶解度比在水中的大,水和四氯化碳互不相溶的性质采用萃取然后分液的方法分离。(5)KNO3晶体中含有少量食盐利用食盐的溶解度受温度的影响变化不大,而KNO3的溶解度受温度的影响变化较大,先把固体溶解在水中,配成高温下的饱和液,然后降低温度,硝酸钾大部分结晶析出,杂质氯化钠仍然溶解在水中,用结晶、重结晶的方法分离提存。所以正确选项为:(1)C (2)E (3)A (4)BE (5)D

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目

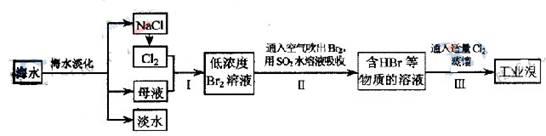
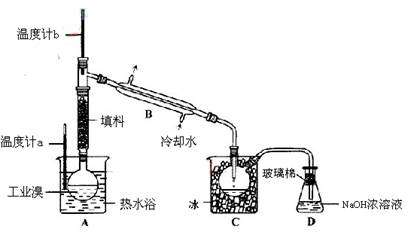

 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是____ ___。
中填写所使用除杂试剂的化学式__________,在( )中的操作名称是____ ___。