题目内容
已知0.1mol某单质与足量的硫在一定条件下充分反应后,质量增加了1.6g,则该单质可能是( )A.钙
B.铜
C.铁
D.铝
【答案】分析:根据金属和硫发生反应的方程式来判断回答.
解答:解:单质与足量的硫的反应属于化合反应,因此质量增加1.6g都是S的质量,则S的物质的量为 =0.05mol,
=0.05mol,
A、发生的反应为:Ca+S=CaS;
B、发生的反应为:2Cu+S=Cu2S;
C、发生的反应为:Fe+S=FeS;
D、发生的反应为:2Al+3S=Al2S3;
当某单质为0.1mol时,消耗S为0.05mol,那么只有Cu满足.
故选B.
点评:本题考查学生硫和金属之间的反应情况,注意硫和金属反应生成的是低价金属的硫化物,可以根据教材知识来回答,难度不大.
解答:解:单质与足量的硫的反应属于化合反应,因此质量增加1.6g都是S的质量,则S的物质的量为
 =0.05mol,
=0.05mol,A、发生的反应为:Ca+S=CaS;
B、发生的反应为:2Cu+S=Cu2S;
C、发生的反应为:Fe+S=FeS;
D、发生的反应为:2Al+3S=Al2S3;
当某单质为0.1mol时,消耗S为0.05mol,那么只有Cu满足.
故选B.
点评:本题考查学生硫和金属之间的反应情况,注意硫和金属反应生成的是低价金属的硫化物,可以根据教材知识来回答,难度不大.

练习册系列答案
相关题目

 I.已知:
I.已知: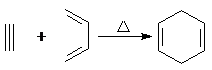 ,如果要合成
,如果要合成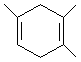 ,所用的原料可以是
,所用的原料可以是