题目内容
【题目】某同学设计了如下装置用于制取SO2并验证SO2的部分性质。回答下列问题:
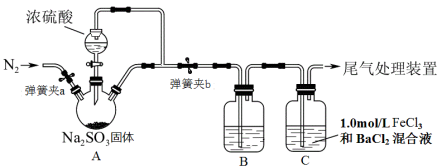
(1)装置A中用于添加浓硫酸的仪器名称为 。
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是:关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到C中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理________。(填“合理”或“不合理”)
(3)实验前要在装置中鼓入N2,目的是 。
(4)为了验证SO2是酸性氧化物,B中可选用的试剂是( )
A.无色酚酞溶液 B.蓝色石蕊试液
C.红色品红溶液 D.KI淀粉混合溶液
(5)装置C中可观察到白色沉淀现象,由此可验证SO2具有 性,相关反应的离子方程式_______。
【答案】(1)滴液漏斗(或分液漏斗,1分)(2)不合理(1分)
(3)排净装置中的空气(1分),防止溶液中SO2被空气中的O2氧化而干扰(1分)(4)B(2分)(5)还原(1分) Ba2++SO2+2Fe3++2H2O=BaSO4↓+4H++2Fe2+(2分)
【解析】
试题分析::(1)根据图示装置可知,盛放浓硫酸的仪器为滴液漏斗或分液漏斗;
(2)检验装置中A、B两部分的气密性,进行的操作是:关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,冷却后长导管中出现一段水柱,说明该装置气密性良好,否则无法判断该装置的气密性是否良好;
(3)氧气、硝酸根离子都能将二氧化硫氧化,所以如果装置中含有氧气,会干扰实验,因此排入氮气的目的是排净空气防止干扰实验;
(4)A.二氧化硫溶液为酸性溶液,不能使无色酚酞溶液变色,无法检验二氧化硫为酸性氧化物,A错误;B.二氧化硫溶液显示酸性,能够使蓝色石蕊试剂变红,可以证明二氧化硫为酸性氧化物,B正确;C.二氧化硫能够使红色品红溶液褪色,证明了二氧化硫漂白性,无法证明二氧化硫为酸性氧化物,C错误;D.KI淀粉混合溶液与二氧化硫不发生反应,无法证明二氧化硫为酸性氧化物,D错误,答案选B;
(5)氯化铁具有氧化性,能够将二氧化硫氧化为硫酸,同时证明二氧化硫具有还原性,反应的离子方程式为Ba2++SO2+2Fe3++2H2O=BaSO4↓+4H++2Fe2+。