题目内容
化工厂的设计是将实验室的研究成果转化为工业化生产的重要的基础工作。
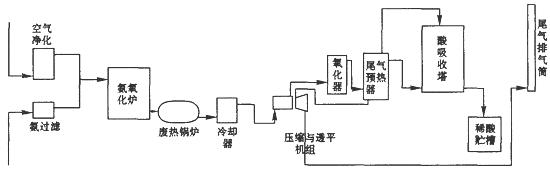
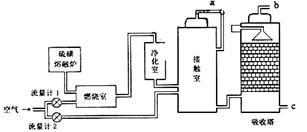
(1)以硫铁矿为原料生产硫酸需经过 、 和 三个主要生产阶段。
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
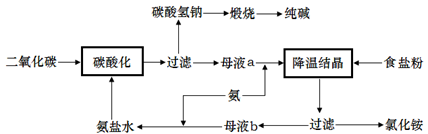
①索尔维制碱法的原理是 。(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 。
③侯氏制碱法可以循环使用的物质有 。
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。
(1)以硫铁矿为原料生产硫酸需经过 、 和 三个主要生产阶段。
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:

①索尔维制碱法的原理是 。(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 。
③侯氏制碱法可以循环使用的物质有 。
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。
(1)二氧化硫炉气的制造、二氧化硫的催化氧化、三氧化硫的吸收
(2)①NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑②侯氏制碱法的工艺由制碱和制氯化铵两个过程组成,形成纯碱与氯化铵的循环
③CO2、NaCl
(3)用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。防止H2与C12混合发生爆炸,同时防止C12-进入阴极室,这样可以获得纯净的NaOH。
试题分析:(1)以硫铁矿为原料生产硫酸需经过硫铁矿的煅烧,二氧化硫炉气的制造、二氧化硫气体的催化氧化、产生的三氧化硫的吸收和硫酸的生成这三个主要生产阶段。(2)①索尔维制碱法的原理是先向饱和的食盐水中通入足量的氨气,然后在通入足量的二氧化碳气体,这时发生反应:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl. 将NaHCO3过滤出来,洗涤干净,然后加热使其发生分解反应:2NaHCO3
 Na2CO3+H2O+CO2↑。即得到了纯碱Na2CO3。②侯氏制碱法与索尔维制碱法相比,优点是侯氏制碱法的工艺由制碱和制氯化铵两个过程组成,形成了纯碱与氯化铵的循环利用,减少了价值不大的CaCl2的生成。③有流程示意图可看出侯氏制碱法可以循环使用的物质有CO2、NaCl。(3)海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是防止阴极室的H2与阳极室C12混合发生爆炸,同时防止C12-进入阴极室,这样可以获得纯净的烧碱——NaOH。
Na2CO3+H2O+CO2↑。即得到了纯碱Na2CO3。②侯氏制碱法与索尔维制碱法相比,优点是侯氏制碱法的工艺由制碱和制氯化铵两个过程组成,形成了纯碱与氯化铵的循环利用,减少了价值不大的CaCl2的生成。③有流程示意图可看出侯氏制碱法可以循环使用的物质有CO2、NaCl。(3)海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是防止阴极室的H2与阳极室C12混合发生爆炸,同时防止C12-进入阴极室,这样可以获得纯净的烧碱——NaOH。
练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目