题目内容
质量为mg的铜与浓H2SO4完全反应,标况下生成气体为VL,则被还原的硫酸是( )
A.
| B.
| C.
| D.
|
发生反应Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,被还有的硫酸生成SO2,
mgCu完全反应,其物质的量=
mol,由方程式可知生成二氧化硫为=
mol,根据S原子守恒可知n被还原(H2SO4)=n(SO2)=
mol,
标况下VL二氧化硫的物质的量=
=
mol,根据S原子守恒可知n被还原(H2SO4)=n(SO2)=
mol,故m被还原(H2SO4)=
mol×98g/mol=
g
故选BC.
| ||
mgCu完全反应,其物质的量=
| m |
| 64 |
| m |
| 64 |
| m |
| 64 |
标况下VL二氧化硫的物质的量=
| V |
| 22.4L/mol |
| V |
| 22.4 |
| V |
| 22.4 |
| V |
| 22.4 |
| 98V |
| 22.4 |
故选BC.

练习册系列答案
相关题目
 +HO-NO2
+HO-NO2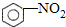 +H2O
+H2O