题目内容
将8.34 g FeSO4·7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)见图。下列说法正确的是( )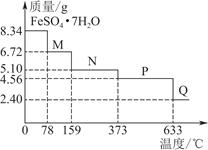
| A.FeSO4·7H2O晶体中有4种不同结合力的水分子 |
| B.在100 ℃时,M的化学式为FeSO4·6H2O |
| C.在200 ℃时,N的化学式为FeSO4·3H2O |
D.380 ℃的P加热至650 ℃的化学方程式为2FeSO4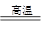 Fe2O3+SO2↑+SO3↑ Fe2O3+SO2↑+SO3↑ |
D
解析

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是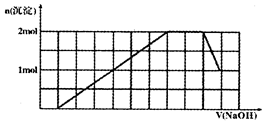
| A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ |
| B.原溶液中一定含有SO42-和Na+ |
| C.原溶液中SO42-的物质的量至少为4.5mol |
| D.反应最后形成的溶液中含有的溶质为Na2SO4 |
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.常温常压下,3.36L NO2和水反应转移的电子数为0.1NA |
| B.1 molNa2O2与足量的水反应,转移的电子数为2NA |
| C.在常温常压下,1molFe与1molCl2充分反应,转移的电子数约为3NA |
| D.在1 L lmol·L-1的氨水中,含有的NH3与NH3·H2O分子的总数小于1mol |
如图是氨气与氯化氢反应的装置。抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )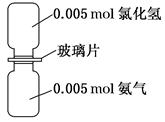
| A.气体反应物的总体积为0.224 L |
| B.生成物的分子个数为0.005NA |
| C.生成物中的N—H键个数为0.02NA |
| D.加水溶解后所得溶液中NH4+数目为0.005NA |
一定体积的溶质质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质的质量分数恰好增大1倍,溶液体积变为62.5 mL。则浓缩后溶液的物质的量浓度为( )。
| A.2.2 mol·L-1 | B.4 mol·L-1 | C.5 mol·L-1 | D.6.25 mol·L-1 |
下列说法中正确的是( )。
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为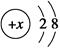 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为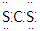 |
| D.中子数为18的氯原子可表示为18Cl |
在(NH4)2Fe(SO4)2溶液中逐滴加入100 mL 1 mol/L的Ba(OH)2溶液,把所得沉淀过滤、洗涤、干燥,得到的固体质量不可能是( )
| A.35.3 g | B.33.5 g | C.32.3 g | D.11.3 g |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| B.在熔融状态下,1 mol NaHSO4完全电离出的阳离子数为2NA |
| C.78 g Na2O2固体与H2O完全反应转移的电子数为NA |
| D.5.6 g铁粉在2.24 L(标准状况)氯气中充分燃烧,失去的电子数为0.3NA |
设NA表示阿伏加德罗常数的数值,下列判断正确的是( )
| A.常温常压下,22.4 L CH4中含有的C—H键数为4NA |
| B.4.6 g由NO2和N2O4组成的混合气体中含有的氧原子数为0.3NA |
| C.含0.2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA |
| D.1 mol Na在足量O2中燃烧生成Na2O2,钠失去的电子数为NA |