题目内容
下列实验操作不能达到实验目的是( )
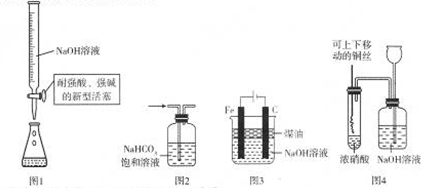

| A、用图1中滴定管准确量取20.00mL NaOH溶液 |
| B、用图2洗气瓶除去二氧化硫中混有的氯化氢 |
| C、用图3装置制备并较长时间观察氢氧化亚铁颜色 |
| D、用图4装置探究铜与浓硝酸反应并体现绿色化学 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.图中为酸式滴定管;
B.二者均与碳酸氢钠溶液反应;
C.Fe为阳极失去电子,阴极上氢离子放电,生成氢氧化亚铁和氢气,且煤油隔绝空气;
D.上下移动的Cu丝可使反应随时停止,盛有NaOH溶液的试剂瓶可处理尾气,并具有缓冲作用,能防止倒吸.
B.二者均与碳酸氢钠溶液反应;
C.Fe为阳极失去电子,阴极上氢离子放电,生成氢氧化亚铁和氢气,且煤油隔绝空气;
D.上下移动的Cu丝可使反应随时停止,盛有NaOH溶液的试剂瓶可处理尾气,并具有缓冲作用,能防止倒吸.
解答:
解:A.图中为酸式滴定管,而NaOH溶液应盛放在碱式滴定管中,故A错误;
B.二者均与碳酸氢钠溶液反应,应利用饱和亚硫酸氢钠溶液来除杂,故B错误;
C.Fe为阳极失去电子,阴极上氢离子放电,生成氢氧化亚铁和氢气,且煤油隔绝空气,则图中装置可制备并较长时间观察氢氧化亚铁颜色,故C正确;
D.上下移动的Cu丝可使反应随时停止,盛有NaOH溶液的试剂瓶可处理尾气,并具有缓冲作用,能防止倒吸,则图中装置可探究铜与浓硝酸反应并体现绿色化学,故D正确;
故选AB.
B.二者均与碳酸氢钠溶液反应,应利用饱和亚硫酸氢钠溶液来除杂,故B错误;
C.Fe为阳极失去电子,阴极上氢离子放电,生成氢氧化亚铁和氢气,且煤油隔绝空气,则图中装置可制备并较长时间观察氢氧化亚铁颜色,故C正确;
D.上下移动的Cu丝可使反应随时停止,盛有NaOH溶液的试剂瓶可处理尾气,并具有缓冲作用,能防止倒吸,则图中装置可探究铜与浓硝酸反应并体现绿色化学,故D正确;
故选AB.
点评:本题考查化学实验方案的评价,为高频考点,把握反应原理及反应装置为解答的关键,涉及常见物质的制备实验及性质实验,注意实验的评价性和操作性分析,题目难度不大.

练习册系列答案
相关题目
造成目前环境污染的因素大体上可分为物理的、化学的与生物的三个方面,它们是造成环境质量下降的主要原因,其中化学物质约占( )
| A、30~40% |
| B、50~60% |
| C、70~80% |
| D、80~90% |
下列说法正确的是( )
| A、毛巾、口罩等个人用品要经常用开水蒸煮,被褥要放在太阳光下直射,其目的都是使病毒蛋白质变性 |
| B、用浓Na2SO4、CuSO4溶液或浓硝酸溶液使蛋清液发生盐析,进而分离、提纯蛋白质 |
| C、蛋白酶是蛋白质,它不仅可以催化蛋白质的水解反应,还可以催化淀粉的水解反应 |
| D、甘氨酸(H2N-CH2-COOH)既有酸性,又有碱性,是最简单的氨基酸 |
已知下列反应热数据,有关分析或说法不正确的是( )
①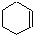 (g)+H2(g)→
(g)+H2(g)→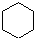 (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1
②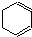 (g)+2H2(g)→
(g)+2H2(g)→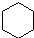 (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1
③ (g)+3H2(g)→
(g)+3H2(g)→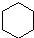 (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.
①
 (g)+H2(g)→
(g)+H2(g)→ (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1②
 (g)+2H2(g)→
(g)+2H2(g)→ (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1③
 (g)+3H2(g)→
(g)+3H2(g)→ (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.| A、上述四种有机物中环已烷最稳定 |
| B、苯分子中不存在独立的碳碳双键 |
| C、1,3-环已二烯比苯稳定 |
| D、苯与H2反应生成1,3-环已二烯吸收热量 |
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
| B、石灰石、生石灰、熟石灰均属于碱 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、Na2O、MgO、Al2O3均属于碱性氧化物 |
把一小块镁、铝合金放入6mol?L-l的NaOH溶液中,可以形成微型原电池.则该电池负极上发生的电极反应为( )
| A、Mg-2e-═Mg2+ |
| B、A1+4OH--3e-═AlO2-+2H2O |
| C、4OH--4e-═2H2O+O2↑ |
| D、2H2O+2e-═2OH-+H2↑ |
下列设备工作时,将化学能转化为热能的是( )
A、 太阳能集热器 |
B、 硅太阳能电池 |
C、 燃气灶 |
D、 锂离子电池 |
 .
.