题目内容
已知下列反应热数据,有关分析或说法不正确的是( )
①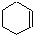 (g)+H2(g)→
(g)+H2(g)→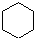 (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1
②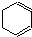 (g)+2H2(g)→
(g)+2H2(g)→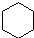 (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1
③ (g)+3H2(g)→
(g)+3H2(g)→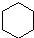 (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.
①
 (g)+H2(g)→
(g)+H2(g)→ (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1②
 (g)+2H2(g)→
(g)+2H2(g)→ (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1③
 (g)+3H2(g)→
(g)+3H2(g)→ (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.| A、上述四种有机物中环已烷最稳定 |
| B、苯分子中不存在独立的碳碳双键 |
| C、1,3-环已二烯比苯稳定 |
| D、苯与H2反应生成1,3-环已二烯吸收热量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、物质的能量越低越稳定;
B、苯分子中是六个介于单键和双键之间的特殊的键;
C、分析反应①②可知,②的△H约是①的2倍,③加成3mol氢气,放热比②还少;
D、据盖斯定律,③-②可得反应.
B、苯分子中是六个介于单键和双键之间的特殊的键;
C、分析反应①②可知,②的△H约是①的2倍,③加成3mol氢气,放热比②还少;
D、据盖斯定律,③-②可得反应.
解答:
解:A、因为环己烷能量最低,所以最稳定,故A正确;
B、苯分子中是六个介于单键和双键之间的特殊的键,故B正确;
C、分析反应①②可知,②的△H约是①的2倍,③加成3mol氢气,放热比②还少,△H=生成物能量-反应物能量,说明苯比1,3-环己二烯能量低,稳定,故C错误;
D、据盖斯定律,③-②可得 (g)+H2(g)→
(g)+H2(g)→ (g)△H=+28.6KJ/mol,故D正确.
(g)△H=+28.6KJ/mol,故D正确.
故选:C.
B、苯分子中是六个介于单键和双键之间的特殊的键,故B正确;
C、分析反应①②可知,②的△H约是①的2倍,③加成3mol氢气,放热比②还少,△H=生成物能量-反应物能量,说明苯比1,3-环己二烯能量低,稳定,故C错误;
D、据盖斯定律,③-②可得
 (g)+H2(g)→
(g)+H2(g)→ (g)△H=+28.6KJ/mol,故D正确.
(g)△H=+28.6KJ/mol,故D正确.故选:C.
点评:本题考查了物质的能量越低越稳定、苯的分子结构、盖斯定律,注意基础知识的学习.

练习册系列答案
相关题目
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、120 mL |
| B、60 mL |
| C、40 mL |
| D、30 mL |
“化学是人类进步的关键”.下列说法不正确的是( )
| A、PM2.5是指空气中直径≤2.5μm的固体颗粒或液滴的总称 |
| B、根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 |
| C、科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的P元素 |
D、 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 |
已知X、Y、Z三种元素的原子核外具有相同的电子层数,且它们的最高价氧化物的水化物酸性依次增强,则下列判断正确的是( )
| A、原子半径按X、Y、Z的顺序增大 |
| B、阴离子的还原性按X、Y、Z顺序增强 |
| C、单质的氧化性按X、Y、Z顺序减弱 |
| D、氢化物的稳定性按X、Y、Z顺序增大 |
在一定温度下,可逆反应A(气)+3B(气)?2C(气)达到平衡的标志是( )
| A、C生成的速率与C分解的速率相等 |
| B、A、B、C的浓度相等 |
| C、A、B、C的分子数比为1:3:2 |
| D、单位时间生成n mol A,同时生成3n mol B |
下列实验操作不能达到实验目的是( )
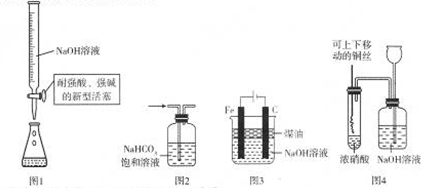

| A、用图1中滴定管准确量取20.00mL NaOH溶液 |
| B、用图2洗气瓶除去二氧化硫中混有的氯化氢 |
| C、用图3装置制备并较长时间观察氢氧化亚铁颜色 |
| D、用图4装置探究铜与浓硝酸反应并体现绿色化学 |
下列实验原理和操作方法可行的是( )
| A、饱和碳酸钠溶液除去CO2气体中混有的SO2 |
| B、用澄清石灰水检验CO气体中混有CO2 |
| C、NO比空气重,可用瓶口向上排气法收集 |
| D、可用萃取、分液提取碘水中的碘 |
下列反应的离子方程式书写正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| B、NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| C、碳酸氢铵溶液和足量氢氧化钠溶液反应:NH4++OH-═NH3?H2O |
| D、NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ |