题目内容
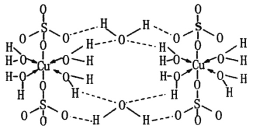
【题目】图为电解精炼银的示意图,电解过程中b电极有少量红棕色气体生成,下列说法不正确的是
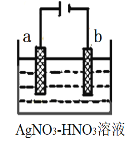
A.a电极是含杂质的粗银
B.溶液中NO![]() 移向a电极
移向a电极
C.b电极的电极反应式为2H++2e=H2↑
D.若b电极增重10.8g,则导线中通过的电子大于0.1mol
【答案】C
【解析】
根据电解精炼粗银的示意图和原理,粗银作阳极,发生氧化反应,除了Ag放电溶解,其余比Ag活泼的金属如Zn等也会放电溶解,纯银作阴极,阴极上主要析出银,还有少量红棕色的二氧化氮气体生成,说明部分硝酸根离子放电,据此分析解答。
A.电解精炼粗银时,粗银为阳极,因此a电极是含杂质的粗银,故A正确;
B.电解池中阴离子向阳极移动,即溶液中NO![]() 移向a电极,故B正确;
移向a电极,故B正确;
C.b极为阴极,主要析出银,有少量红棕色气体生成,该气体为NO2,电极反应式一定不是2H++2e-=H2↑,故C错误;
D.当纯银片增重10.8 g时,说明阴极析出0.1 molAg,根据电极反应式Ag++e-=Ag,析出0.1molAg导线中通过的电子为0.1mol,由于b极上有少量红棕色气体生成,说明b极上还有硝酸根得电子被还原成NO2,则电路中通过的电子数目大于0.1 mol,故D正确;
故选C。

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目
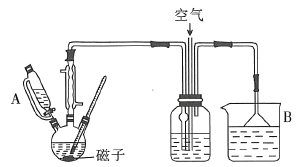
【题目】现向下列装置中缓慢通入气体X,分别进行关闭和打开活塞K的操作,则品红溶液和澄清石灰水中现象相同的一组是
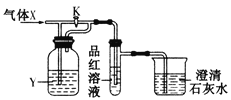
选项 | A | B | C | D |
X | NO2 | SO2 | Cl2 | CO2 |
Y(过量) | 浓H2SO4 | NaHCO3饱和溶液 | Na2SO3溶液 | NaHSO3饱和溶液 |
A.AB.BC.CD.D