题目内容
【题目】结合氯气的相关知识解决下列问题。
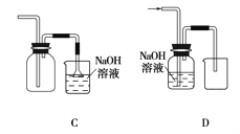
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______(填字母)。

漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为_________________________。漂白粉与浓盐酸发生氧化还原反应,化学方程式为____________________________________。
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
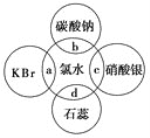
①能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
②c过程中的现象是________________。
【答案】C Ca(ClO)2+2HCl=CaCl2+2HClO Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O d 产生白色沉淀
【解析】
(1)氯气是比空气重的可溶于水的有毒气体,依据氯气物理性质和装置分析;盐酸酸性强于次氯酸,漂白粉与稀盐酸反应生成氯化钙和次氯酸;次氯根离子具有强的氧化性,能够氧化浓盐酸,二者发生归中反应生成氯气,依据得失电子守恒、原子个数守恒书写方程式;
(2)将氯气溶于水得到氯水(浅黄绿色),氯水含多种微粒,其中有H2O、Cl2、HClO、Cl-、H+、OH-(极少量,水微弱电离出来的)。
氯水的性质取决于其组成的微粒:
①漂白、消毒性:氯水中的Cl2和HClO均有强氧化性,一般在应用其漂白和消毒时,应考虑HClO,HClO的强氧化性将有色物质氧化成无色物质,不可逆;
②沉淀反应:加入AgNO3溶液有白色沉淀生成(氯水中有Cl-)。
(1)氯气是比空气重的可溶于水的有毒气体;
A.导气管位置正确,因为氯气比空气重用向上排气方法,但只有进气口,无出气口,无法排出气体,A错误;
B.此装置是用来收集比空气轻的气体,若收集氯气,需要短进长出,B错误;
C.装置长进短出可以收集比空气重的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,C正确;
D.氯气通入NaOH溶液会发生反应.氯气被氢氧化钠吸收,不能收集到氯气,D错误;
故合理选项是C;
盐酸酸性强于次氯酸,漂白粉与稀盐酸反应生成氯化钙和次氯酸,方程式:Ca(ClO)2+2HCl=CaCl2+2HClO;
次氯根离子具有强的氧化性,能够氧化浓盐酸,次氯酸钙与盐酸发生氧化还原反应生成氯气、氯化钙和水,方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)①氯水中的HClO有强氧化性,一般在应用其漂白时,HClO的强氧化性将有色物质氧化成无色物质,本题中氯水能使石蕊试液先变红,后褪色,故合理选项是d;
②氯水中有Cl-,加入AgNO3溶液,发生反应:Ag++Cl-=AgCl↓,生成AgCl白色沉淀。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】将0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是( )
2Fe2++I2”的是( )
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
已知:离子方程式:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓(蓝色沉淀)
A.①B.②和④C.③和④D.①和②