题目内容
【题目】镁带能在CO2中燃烧,生成氧化镁和单质碳。请完成下列填空:
(1)碳元素形成的单质有金刚石、石墨、足球烯等。金刚石的熔点远高于足球烯的原因是_______。
(2)氧化镁的电子式为_______,CO2的结构式为______。与镁同周期、离子半径最小的元素,其原子最外层的电子排布式为______,其1个原子中能量最高的电子有______个。
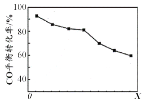
(3)一定条件下,在容积恒为2.0L的容器中,Fe和CO2发生如下反应:CO2(g)+Fe(s)![]() FeO(s)+CO(g),若起始时向容器中加入1molCO2,5.0min后,容器内气体的相对平均分子量为32,则n(CO2):n(CO)之比为_______,这段时间内用CO2表示的速率v(CO2)=_______。
FeO(s)+CO(g),若起始时向容器中加入1molCO2,5.0min后,容器内气体的相对平均分子量为32,则n(CO2):n(CO)之比为_______,这段时间内用CO2表示的速率v(CO2)=_______。
(4)下列说法错误的是_______。
a.当混合气体的密度不变时说明反应达到了平衡
b.混合气体的平均相对分子质量不变时说明反应达到了平衡
c.平衡后移除二氧化碳时,正反应速率一直减小直至建立新的平衡
d.平衡后缩小容器的体积,正逆反应速率不变,平衡不移动
(5)保持温度不变的情况下,待反应达到平衡后再充入一定量的二氧化碳,平衡向______移动(选填“正向”、“逆向”、或“不”),二氧化碳的转化率_____(填“增大”,“减小”或“不变”)。
【答案】金刚石为原子晶体而足球烯为分子晶体,金刚石中共价键的键能高于足球烯中的分子间作用力,故金刚石的熔点远高于足球烯 ![]() O=C=O 3s23p1 1 1:3 0.075mol/(L·min) c、d 正向 不变
O=C=O 3s23p1 1 1:3 0.075mol/(L·min) c、d 正向 不变
【解析】
(1)金刚石为原子晶体而足球烯为分子晶体,金刚石中共价键的键能高于足球烯中的范德华力;
(2)氧化镁的电子式为![]() ;CO2中碳和氧共用四对电子,所以结构式是O=C=O;第三周期元素中,离子电子层数越少,核电荷数越大,其离子半径越小,所以离子半径最小的是Al3+;
;CO2中碳和氧共用四对电子,所以结构式是O=C=O;第三周期元素中,离子电子层数越少,核电荷数越大,其离子半径越小,所以离子半径最小的是Al3+;
(3)CO2(g)+Fe(s) ![]() FeO(s)+CO(g)是气体体积不变的反应,5.0min后,容器内气体是总物质的量为1mol的CO和CO2混合气体,设CO的物质的量为xmol,CO2的物质的量为(1-x)mol,相对平均分子量为
FeO(s)+CO(g)是气体体积不变的反应,5.0min后,容器内气体是总物质的量为1mol的CO和CO2混合气体,设CO的物质的量为xmol,CO2的物质的量为(1-x)mol,相对平均分子量为![]() =32g/mol,以此解答;
=32g/mol,以此解答;
(4)根据反应到达平衡的特征回答;
(5)待反应达到平衡后再充入一定量的二氧化碳,平衡向正向移动,但到达新平衡时的效果与原平衡等效,故二氧化碳的转化率不变。
(1)金刚石为原子晶体而足球烯为分子晶体,金刚石中共价键的键能高于足球烯中的范德华力,故熔点金刚石大于石墨烯;
(2)氧化镁的电子式为![]() ;CO2中碳和氧共用四对电子,所以结构式是O=C=O;第三周期元素中,离子电子层数越少,核电荷数越大,其离子半径越小,所以离子半径最小的是Al3+,Al原子核外最外层电子数是3且位于第三电子层上,所以Al原子价电子排布式为3s23p1;在含多个电子的原子中,能量最高的电子是离原子核最远的电子,Al原子中能量最高的电子有1个;
;CO2中碳和氧共用四对电子,所以结构式是O=C=O;第三周期元素中,离子电子层数越少,核电荷数越大,其离子半径越小,所以离子半径最小的是Al3+,Al原子核外最外层电子数是3且位于第三电子层上,所以Al原子价电子排布式为3s23p1;在含多个电子的原子中,能量最高的电子是离原子核最远的电子,Al原子中能量最高的电子有1个;
(3)CO2(g)+Fe(s) ![]() FeO(s)+CO(g)是气体体积不变的反应,5.0min后,容器内气体是总物质的量为1mol的CO和CO2混合气体,设CO的物质的量为xmol,CO2的物质的量为(1-x)mol,相对平均分子量为
FeO(s)+CO(g)是气体体积不变的反应,5.0min后,容器内气体是总物质的量为1mol的CO和CO2混合气体,设CO的物质的量为xmol,CO2的物质的量为(1-x)mol,相对平均分子量为![]() =32g/mol,解得x=0.75,则CO的物质的量为0.75mol,CO2的物质的量为0.25mol,n(CO2):n(CO)之比为1:3;这段时间内用CO2表示的速率v(CO2)=
=32g/mol,解得x=0.75,则CO的物质的量为0.75mol,CO2的物质的量为0.25mol,n(CO2):n(CO)之比为1:3;这段时间内用CO2表示的速率v(CO2)= 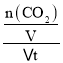 =
=  =0.075mol/(L·min);
=0.075mol/(L·min);
(4)a. CO2(g)+Fe(s) ![]() FeO(s)+CO(g)是气体体积不变的反应,当混合气体的密度不变时说明,混合气体的质量不变,说明应该达到平衡,正确;
FeO(s)+CO(g)是气体体积不变的反应,当混合气体的密度不变时说明,混合气体的质量不变,说明应该达到平衡,正确;
b. CO2(g)+Fe(s) ![]() FeO(s)+CO(g)是气体总物质的量不变的反应,混合气体的平均相对分子质量不变时,混合气体的质量不变,说明应该达到平衡,正确;
FeO(s)+CO(g)是气体总物质的量不变的反应,混合气体的平均相对分子质量不变时,混合气体的质量不变,说明应该达到平衡,正确;
c. 平衡后移除二氧化碳时,正反应速率先减小后增大,直至建立新的平衡,故错误;
d.平衡后缩小容器的体积,正逆反应速率增大,但平衡不移动,故错误;
错误的是c、d;
(5)待反应达到平衡后再充入一定量的二氧化碳,平衡向正向移动,但到达新平衡时的效果与原平衡等效,故二氧化碳的转化率不变;

 阅读快车系列答案
阅读快车系列答案【题目】除去下列物质中所含杂质(括号中的物质)所选用的试剂和装置均正确的是( )
Ⅰ.试剂:①KMnO4酸性溶液 ②NaOH溶液 ③饱和Na2CO3溶液 ④H2O ⑤Na ⑥溴水 ⑦Br2的CCl4溶液
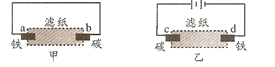
Ⅱ.装置:

选项 | 物质 | 试剂 | 装置 |
A | C2H6(C2H4) | ⑥ | ① |
B | 苯(苯酚) | ① | ③ |
C | CH3COOC2H5(CH3COOH) | ③ | ② |
D | 甲苯(二甲苯) | ⑦ | ④ |
A.AB.BC.CD.D
【题目】(1)用O2将HCl转化为Cl2,可提高效益,减少污染.传统上该转化通过如图所示的催化剂循环实现,其中,反应①为 2HCl(g)+CuO(s)=H2O(g)+CuCl2(s) ![]() 反应②生成1molCl2(g)的反应热为
反应②生成1molCl2(g)的反应热为![]() ,则总反应的热化学方程式为_______________(反应热△H用含
,则总反应的热化学方程式为_______________(反应热△H用含![]() 和
和![]() 的代数式表示)。
的代数式表示)。
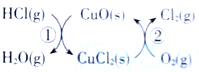
(2)在容积为1L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
①该反应的![]() ____________0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如下表所示。在0~60s时段,反应速率υ(N2O4)为_________mol·L-1·s-1;40s时C2___________0.10mol/L(填“>”或“<”)。
____________0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如下表所示。在0~60s时段,反应速率υ(N2O4)为_________mol·L-1·s-1;40s时C2___________0.10mol/L(填“>”或“<”)。
②100℃时达平衡后,改变反应温度为![]() ,c(N2O4)以0.0020 mol·L
,c(N2O4)以0.0020 mol·L![]() ·s
·s![]() 的平均速率降低,经10s又达到平衡。则T______100℃(填“>”或“<”)。
的平均速率降低,经10s又达到平衡。则T______100℃(填“>”或“<”)。
③计算温度T时反应的平衡常数K___________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半。平衡向___________(填“正反应”或“逆反应”)方向移动,N2O4的转化率______(填“增大”或“减小”)。
时间(s) | 0 | 20 | 40 | 60 | 80 |
N2O4浓度 (mol/L) | 0.10 | 0.06 | C1 | 0.04 | 0.04 |
NO2浓度 (mol/L) | 0 | 0.08 | C2 | 0.12 | 0.12 |