题目内容
19.下列实验操作中,所用仪器合理的是( )| A. | 用25mL的烧杯量取14.80mL NaOH溶液 | |
| B. | 用100mL的量筒量取5.2mL的盐酸 | |
| C. | 用托盘天平称取25.20g NaCl | |
| D. | 用100mL容量瓶配制80mL 0.1mol/L的盐酸 |
分析 A.烧杯不能精确量取溶液;
B.100mL 量筒精确到1mL;
C.托盘天平的精确度为0.1g;
D.100mL容量瓶只能配制100mL盐酸.
解答 解:A.烧杯不能精确量取溶液,应用碱式滴定管,故A错误;
B.100mL 量筒精确到1mL,无法量取5.2mL 盐酸,故B错误;
C.托盘天平称取25.20gNaCl固体是不合理的,数据25.20gNaCl不符合的精确度为0.1g,故C错误;
D.容量瓶只有一个刻度,100mL容量瓶能配制100mL盐酸,然后量取80mL,故D正确.
故选D.
点评 本题考查中学化学中常用仪器在使用中读数的问题,难度不大,配制一定物质的量浓度的溶液,学生应熟悉不同仪器的精确度不同并熟练掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.Ⅰ、氯气在298K、100kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应.请回答下列问题:
(1)氯水久置后会变质,请分析变质的原因.(请用方程式及必要文字说明分析)氯气与水反应:H2O+Cl2?HCl+HClO,HClO不稳定分解:2HClO═2HCl+O2↑
(2)如果增大氯气的压强,氯气在水中的溶解度将增大(填“增大”“减小”或“不变”)
Ⅱ、在2L恒容的密闭容器中,加入4mol SO3(g),在某温度下使其反应,反应至4min时,氧气的浓度为0.5mol/L,当反应到8min时,反应到达平衡.
(1)0min~4min内生成O2的平均速率:v(O2)=0.125mol/(L•min).
(2)若8分钟达到平衡时,测得SO3浓度为0.04mol/L.若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.04mol/L的是BD
(1)氯水久置后会变质,请分析变质的原因.(请用方程式及必要文字说明分析)氯气与水反应:H2O+Cl2?HCl+HClO,HClO不稳定分解:2HClO═2HCl+O2↑
(2)如果增大氯气的压强,氯气在水中的溶解度将增大(填“增大”“减小”或“不变”)
Ⅱ、在2L恒容的密闭容器中,加入4mol SO3(g),在某温度下使其反应,反应至4min时,氧气的浓度为0.5mol/L,当反应到8min时,反应到达平衡.
(1)0min~4min内生成O2的平均速率:v(O2)=0.125mol/(L•min).
(2)若8分钟达到平衡时,测得SO3浓度为0.04mol/L.若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.04mol/L的是BD
| A | B | C | D | |
| SO3 | 0mol | 4mol | 2mol | 0mol |
| SO2 | 4mol | 1.5mol | 0mol | 4mol |
| O2 | 2mol | 0mol | 0mol | 4mol |
10.下列离子方程式正确的是( )
| A. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2 H+=2 H2O+I2 | |
| C. | 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓ | |
| D. | 高锰酸钾酸性溶液吸收二氧化硫:SO2+MnO4-+4H+=SO42-+Mn2++2H2O |
7.下列化学用语表达正确的是( )
| A. | CO2分子比例模型: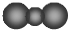 | |
| B. | 氨基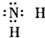 | |
| C. | 原子结构示意图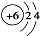 表示12C,也可以表示14C 表示12C,也可以表示14C | |
| D. | 乙炔的最简式 CH≡CH |
14.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )
| A. | 再通入少量氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 | |
| B. | 加入少量的碳酸钠粉末,pH增大,溶液漂白性增强 | |
| C. | 加入少量固体NaOH,一定有c(Na+)═c( Cl-)+c(ClO- ) | |
| D. | 加入少量水,水的电离平衡向逆反应方向移动 |
11.下列说法中正确的是( )
①自然界中不存在游离态的硫
②将氯气通入石蕊试液先变红后褪色,将SO2通入石蕊试液也能褪色.
③二氧化硫的排放会导致光化学烟雾的产生
④二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
⑤向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
⑥浓硫酸可用来干燥SO2、CO、C12等气体
⑦将SO2通入硝酸钡溶液,生成白色沉淀BaSO3
⑧SiO2有导电性,所以可用于制光导纤维.
①自然界中不存在游离态的硫
②将氯气通入石蕊试液先变红后褪色,将SO2通入石蕊试液也能褪色.
③二氧化硫的排放会导致光化学烟雾的产生
④二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
⑤向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
⑥浓硫酸可用来干燥SO2、CO、C12等气体
⑦将SO2通入硝酸钡溶液,生成白色沉淀BaSO3
⑧SiO2有导电性,所以可用于制光导纤维.
| A. | ①③⑤⑦ | B. | ⑥ | C. | ①②③④⑤⑦⑧ | D. | ②④⑥⑧ |
8.下列化学用语正确的是( )
| A. | 甲烷的球棍模型: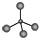 | B. | 羟基的电子式: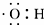 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 乙酸的结构简式C2H4O2 |
 .
.