题目内容
【题目】A、B、C、D四物质有如下转化关系(反应条件和部分产物已略去):A![]() B
B![]() C
C![]() D,回答下列问题:
D,回答下列问题:
(1)若A为气态氢化物和D能通过化合反应生成一种盐,则
①写出实验室制取A的化学方程式:______________________________________;
②写出由A生成B的化学方程式:______________________________________;
③某同学用干燥的圆底烧瓶收集一瓶A气体,用滴入酚酞的水做喷泉实验,能观察到美丽的红色喷泉。用方程式解释喷泉呈红色的原因:_____________________________________________。
(2)若A与B反应能生成一种淡黄色固体单质,写出该反应的化学方程式:_______________________。
(3)若A是金属单质,C是一种淡黄色固体,写出C生成D的离子方程式:____________。
【答案】Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O 4NH3+5O2
CaCl2+2NH3↑+2H2O 4NH3+5O2![]() 4NO+6H2O NH3+H2O
4NO+6H2O NH3+H2O ![]() H3·H2O
H3·H2O![]() NH4++OH- SO2+2H2S=3S↓+2H2O 2Na2O2+2H2O=4Na++4OH-+O2↑
NH4++OH- SO2+2H2S=3S↓+2H2O 2Na2O2+2H2O=4Na++4OH-+O2↑
【解析】
(1) A为气态氢化物和D能通过化合反应生成一种盐,则A是NH3,B是NO,C是NO2,D是HNO3;
(2)若A与B反应能生成一种淡黄色固体单质,则A是H2S,B是SO2,C是H2SO3;
(3)若A是金属单质,C是一种淡黄色固体,则A是Na,B是Na2O,C是Na2O2,D是NaOH。据此分析解答。
(1)①若A为气态氢化物和D能通过化合反应生成一种盐,则A是碱性气体NH3,B是NO,C是NO2,D是HNO3。在实验室中是用铵盐NH4Cl和熟石灰Ca(OH)2在加热条件下反应制取氨气的,反应方程式为Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
②NH3与O2在催化剂存在时,在加热条件下发生氧化还原反应,产生NO和水,反应的化学方程式为4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
③氨气极容易溶于水,溶于水的氨气绝大多数与水发生反应产生一水合氨,NH3+H2O![]() NH3H2O,产生的一水合氨又有少部分发生电离:NH3H2O
NH3H2O,产生的一水合氨又有少部分发生电离:NH3H2O![]() NH4++OH-,产生OH-,使溶液显碱性,因此溶液中若滴有酚酞试液,溶液变为红色;
NH4++OH-,产生OH-,使溶液显碱性,因此溶液中若滴有酚酞试液,溶液变为红色;
(2)若A与B反应能生成一种淡黄色固体单质,则A是H2S,B是SO2,A与B在室温下混合,发生反应:2H2S+SO2=3S↓+2H2O,
C是H2SO3;
(3)若A是金属单质,C是一种淡黄色固体,则A是金属Na,B是Na2O,C是Na2O2,D是NaOH。,Na2O2与水反应产生NaOH和氧气,则C生成D的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑。

【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
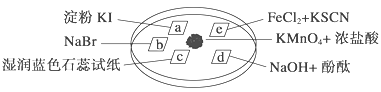
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D