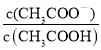题目内容
【题目】常温下,用0.1 mol·L-1的CH3COOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴加V mL CH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是( )
A.Ka=![]() B.V=
B.V=![]() C.Ka=
C.Ka=![]() D.Ka=
D.Ka=![]()
【答案】A
【解析】
常温下,用0.1 mol·L-1的CH3COOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴加V mL CH3COOH溶液时,混合溶液的pH=7。则c(OH-) = c(H+) =1×10-7 mol·L-1,c(Na+) =c(CH3COO-) =![]() ,因此CH3COOH的电离平衡常数为
,因此CH3COOH的电离平衡常数为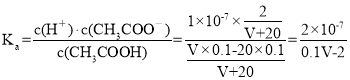 ,故A正确。
,故A正确。
综上所述,答案为A。

练习册系列答案
相关题目