题目内容
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:

下列说法不正确的是
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.如图中△H1=△H2+△H3

D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH2e![]()
![]() +2H2O
+2H2O
【答案】C
【解析】本题考查热化学知识和盖斯定律的应用。A.通过太阳能实现总反应:H2O+CO2→H2+CO+O2,CeO2没有消耗,CeO2是光催化剂,故A正确;B.该过程中在太阳能作用下将H2O、CO2转变为H2、CO,所以把太阳能转变成化学能,故B正确;C.由图可知,根据盖斯定律,应该是:△H1=△H2+△H3;故C错误;D.CO在负极失电子生成CO2,在碱性条件下再与OH生成![]() ,故负极反应式正确;故D正确;故选C。
,故负极反应式正确;故D正确;故选C。

【题目】⑴为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中。
实验要求 | 化学试剂 |
检验酒精中是否有水 | _____ |
区别CH4和C2H4两种无色气体 | _____ |
验证味精是否有食盐 | _____ |
除去Fe2O3中的Al2O3 | _____ |
供选择的化学试剂:
A.酸性高锰酸钾 B.硝酸银溶液和硝酸 C.氢氧化钠溶液 D.无水硫酸铜粉末
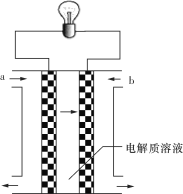
⑵红热木炭与浓H2SO4反应的化学方程式是 C+2H2SO4 ![]() CO2↑+2SO2↑+2H2O ,该反应中浓硫酸的作用是___________________。按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2。已知图中4个洗气瓶均装有检测液。现给出4种溶液①品红溶液②酸性高锰酸钾溶液③品红溶液④澄清石灰水。试回答下列问题。
CO2↑+2SO2↑+2H2O ,该反应中浓硫酸的作用是___________________。按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2。已知图中4个洗气瓶均装有检测液。现给出4种溶液①品红溶液②酸性高锰酸钾溶液③品红溶液④澄清石灰水。试回答下列问题。
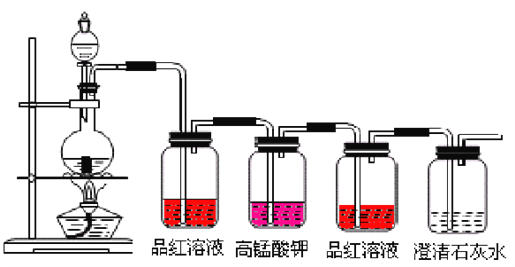
第一个洗气瓶中品红溶液褪色,体现了二氧化硫具有________________性。
第一个洗气瓶的作用是______________________________________________。
第二个洗气瓶中高锰酸钾溶液褪色,体现了二氧化硫具有______________性。