题目内容
【题目】工业上用某矿渣(含有Cu2O、Al2O3,Fe2O3、SiO2)制取铜的操作流程如下:
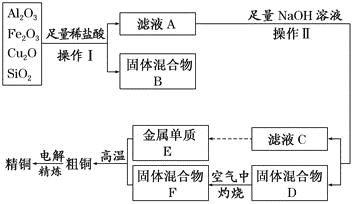
已知:Cu2O+2H+= Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为 ;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有 (填仪器名称)。
(2)滤液A中铁元素的存在形式为 (填离子符号),生成该离子的离子方程式为 ,检验滤液A中存在该离子的试剂为 (填试剂名称)。
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为 。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH= 。
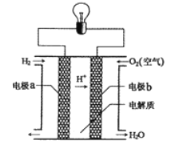
(5)利用电解法进行粗铜精炼时,下列叙述正确的是 (填代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
(6)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→ →过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,说出主要操作方法,不必描述操作过程的细节)
【答案】(1)过滤;坩埚;
(2)Fe2+;Cu+2Fe3+===Cu2++2Fe2+;硫氰化钾溶液和新制氯水或铁氰化钾溶液;
(3)2Al+Fe2O3![]() 2Fe+Al2O3;(4)11;
2Fe+Al2O3;(4)11;
(5)b c;(6)将浓硫酸用蒸馏水稀释,使样品与足量稀硫酸充分反应。
【解析】试题分析:(1)操作I得到液体和固体,因此操作步骤为过滤;灼烧固体需要在坩埚中进行,因此缺少的是坩埚;
(2)Cu2O在酸性条件生成Cu,Fe2O3+6H+=2Fe3++3H2O,Cu+2Fe3+=Cu2++2Fe2+,因此铁元素以Fe2+形式存在;检验Fe2+:先加KSCN溶液,观察溶液颜色,然后再加氯水,如果溶液变为红色,说明含有Fe2+,也可以用K3Fe(CN)6,如果产生蓝色沉淀,说明有Fe2+;
(3)焊接钢轨,采用铝热反应,即2Al+Fe2O3![]() 2Fe+Al2O3;
2Fe+Al2O3;
(4)设pH=x,NaOH溶液中水电离出c(OH-)=c(H+)=10-x,则NaAlO2中水电离的c(OH-)=10(8-x),NaAlO2的pH=10-14/10(8-x)=10(x-22),两者pH相等,则有x=22-x,解得x=11;
(5)a、电解过程一部分能量转化成热能,故错误;b、精炼铜时,粗铜作阳极,发生氧化反应,纯铜作阴极,化合价降低,发生还原反应,故正确;c、粗铜中含有锌、铁等杂质,Zn-2e-=Zn2+,阴极上:Cu2++2e-=Cu,溶液Cu2+略有降低,故正确;d、阴极:Cu2++2e-=Cu,能够得到通过的电量和析出铜的量的关系,故错误;(6) 将浓硫酸用蒸馏水稀释,使样品与足量稀硫酸充分反应。

【题目】“C化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH=-49.0 kJ/mol。相关数据如下:
CH3OH(g) + H2O(g) ΔH=-49.0 kJ/mol。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 1 mol CH3OH(g)和1 mol H2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4 kJ | 吸收a kJ |
请回答:①c1 c2(填“>”、“<”或“=”);a= 。
②若甲中反应达到平衡耗时10 s,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是_____mol/(L·s)。
(2)向体积为1 L的密闭容器中充入b mol CO和2b mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g)。平衡时CO的转化率与温度的关系如图所示。请回答下列问题:
CH3OH(g)。平衡时CO的转化率与温度的关系如图所示。请回答下列问题:

①正反应属于 (填“吸”或“放”)热反应。
②100℃时,该反应的平衡常数K= (用含b的代数式表示)。
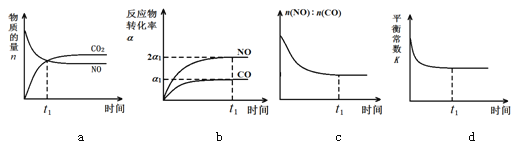
(3)治理汽车尾气的反应是2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母)
2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母)
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为________,氧化性最弱的简单阳离子是________。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是_______________________________ ___;
制铝时,电解Al2O3而不电解AlCl3的原因是____________________________ __。
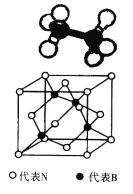
(4)晶体硅(熔点1410 ℃)是良好的半导体材料,SiCl4(熔点-70 ℃)。由粗硅制纯硅过程如下:
![]()
SiCl4属于 晶体。在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:______________________________________ 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是________。
a.NH3b.HI c.SO2d.CO2