��Ŀ����
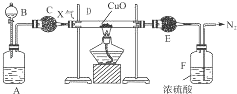
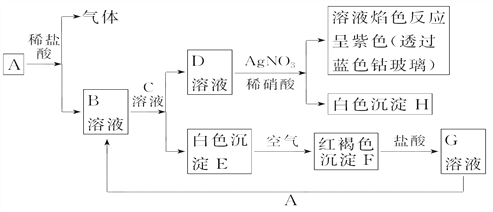
����Ŀ��������û����ɫ���д̼�����ζ�����壬��������ˮ���ܽ�ÿ죬1���ˮ��Լ���ܽ�700�����������ʵ����������Ȼ�狀��������ƹ�����ȡ������ijͬѧ������װ�ý����йذ�����ȡ����Ȫʵ���̽������ش�
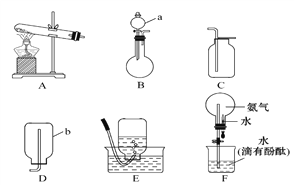
(1)д��ͼ����ʾ���������ƣ�a____________��b____________��
(2)ʵ������ȡ�����Ļ�ѧ����ʽΪ_____________________________________����ͼ��ѡ����Ӧ�ķ���װ����________(����ĸ����ͬ)���ռ�װ����________��
(3)ijͬѧ���ռ��и��﴿��������Fװ�ý���ʵ��۲쵽�˺�ɫ��Ȫ�����������Ĺؼ�������_______________________________________________��
(4)0�桢101 kPa��������ʵ���������ƿ����Һ���ʵ����ʵ���Ũ��Ϊ(������NH3����)��____________��
���𰸡� ��Һ©�� ����ƿ 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O A�� D�� ���ἷѹ��ͷ�ιܣ�ʹ����ˮ������ƿ��Ȼ���ֹˮ��
CaCl2+2NH3��+2H2O A�� D�� ���ἷѹ��ͷ�ιܣ�ʹ����ˮ������ƿ��Ȼ���ֹˮ�� ![]() mol��L-1
mol��L-1
����������1�������������ص�ȷ�����������ƣ�a�Ƿ�Һ©����b�Ǽ���ƿ����2���ڼ��������£��Ȼ�狀��������Ʒ�Ӧ�����Ȼ��ơ�������ˮ������ʽΪ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O����Ӧ���ǹ��壬��Ҫ��������ȡ���������ѡ��װ��A������������ˮ���ܶ�С�ڿ��������Բ��������ſ������ռ�����ѡ��Dװ�ã���3��NH3�����ܽ���ˮ��1���ˮ�ܽ�700�����������ֹˮ�м�����ͷ�ι��е�ˮ��Ȼ���ֹˮ��K�����ڰ���Ѹ���ܽ��ڼ�����ͷ�ι��е�ˮ��������ƿ������ѹǿѸ�ټ�С������ˮ������ƿ������Ȫ����4��������֪�����ð�ˮ������ƿ������ƿ�������V����ˮ��Һ��Ũ��c��NH3����
CaCl2+2NH3��+2H2O����Ӧ���ǹ��壬��Ҫ��������ȡ���������ѡ��װ��A������������ˮ���ܶ�С�ڿ��������Բ��������ſ������ռ�����ѡ��Dװ�ã���3��NH3�����ܽ���ˮ��1���ˮ�ܽ�700�����������ֹˮ�м�����ͷ�ι��е�ˮ��Ȼ���ֹˮ��K�����ڰ���Ѹ���ܽ��ڼ�����ͷ�ι��е�ˮ��������ƿ������ѹǿѸ�ټ�С������ˮ������ƿ������Ȫ����4��������֪�����ð�ˮ������ƿ������ƿ�������V����ˮ��Һ��Ũ��c��NH3����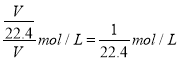 ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ�����з�����ᴿ��ʵ���У���ѡ�õķ�������������ȷ���ǣ� ��
��� | A | B | C | D |
ʵ��Ŀ�� | ��ȡ����ˮ | ����ˮ��ֲ���� | ����ʳ��ˮ����ɳ | ��Ũʳ��ˮ�еõ��Ȼ��ƾ��� |
���뷽�� | ���� | ��Һ | ��ȡ | ���� |
ѡ������ |
|
|
|
|
A.ѡ��A
B.ѡ��B
C.ѡ��C
D.ѡ��D
����Ŀ��������Ԫ��W��X��Y��Z�����ڱ��е����λ�������ʾ��������Ԫ��ԭ�ӵ����������֮��Ϊ21�����й�ϵ��ȷ���ǣ�������
W | X | |||
Y | Z |
A. �⻯��е㣺W��Z
B. �������Ӧˮ��������ԣ�Y��W
C. Y2X3��YZ3������������ͬ
D. �����ӵİ뾶��Y��X