题目内容
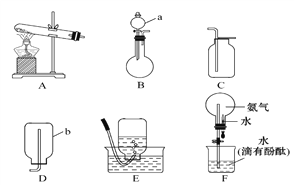
【题目】如图是某气体X产生并研究其性质的装置. 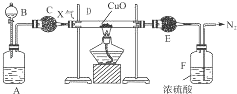
A中盛有微溶的白色固体,B中盛有无色挥发性液体,C和E中盛有干燥剂.A和B中物质相遇时有无色气体X生成,它经图中一系列装置在末端得到N2 , 且E管的质量增加.
(1)写出盛放试剂的名称: A. , B. , C. , E. .
(2)A和B中物质相遇生成X的主要原因是: .
(3)D中反应的化学方程式 .
(4)F中反应的化学方程式 .
(5)从D中反应说明气体X具有(填“酸性”“碱性”“氧化性”或“还原性”).
【答案】
(1)生石灰;浓氨水;碱石灰;碱石灰
(2)CaO与水化合生成熟石灰,消耗水并放出大量热,使浓氨水中的NH3逸出
(3)3CuO+2NH3 ![]() N2+3Cu+3H2O
N2+3Cu+3H2O
(4)2NH3+H2SO4═(NH4)2SO4
(5)还原性
【解析】解:从末端的N2逆推可知X中含N元素.从E增重可推导D中反应有水生成.N2和H2O均由D中反应而来,初步判断D中CuO与含N、H元素的物质X作用,猜想X为NH3 . A、B相遇得NH3 , B应盛有浓氨水,A中应盛固体NaOH或CaO,因题给物质微溶,可知它是CaO.(1)分析可知ABCE中盛放试剂的名称分别为:生石灰; 浓氨水;碱石灰; 碱石灰,所以答案是:生石灰; 浓氨水;碱石灰; 碱石灰;(2)A和B中物质相遇生成X的主要原因是CaO与水化合生成熟石灰,消耗水并放出大量热,使浓氨水中的NH3逸出,所以答案是:CaO与水化合生成熟石灰,消耗水并放出大量热,使浓氨水中的NH3逸出;(3)D中反应是氨气和氧化铜加热发生的氧化还原反应生成氮气、铜和水,反应的化学方程式为:3CuO+2NH3 ![]() N2+3Cu+3H2O,所以答案是:3CuO+2NH3
N2+3Cu+3H2O,所以答案是:3CuO+2NH3 ![]() N2+3Cu+3H2O;(4)F中的反应是氨气和浓硫酸反应生成硫酸铵,反应的化学方程式为:2NH3+H2SO4═(NH4)2SO4 , 所以答案是:2NH3+H2SO4═(NH4)2SO4 ;(5)氨气和氧化铜反应3CuO+2NH3
N2+3Cu+3H2O;(4)F中的反应是氨气和浓硫酸反应生成硫酸铵,反应的化学方程式为:2NH3+H2SO4═(NH4)2SO4 , 所以答案是:2NH3+H2SO4═(NH4)2SO4 ;(5)氨气和氧化铜反应3CuO+2NH3 ![]() N2+3Cu+3H2O,反应过程中氨气中 氮元素化合价﹣3价变化为0价,氨气表现为还原性所以答案是:还原性.
N2+3Cu+3H2O,反应过程中氨气中 氮元素化合价﹣3价变化为0价,氨气表现为还原性所以答案是:还原性.