题目内容
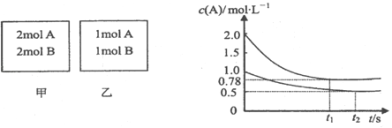
【题目】向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同温度下,发生反应:A(g)+B(g)xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
A.x可能等于2
B.甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙)
C.将乙容器升温可使甲、乙容器内各物质的体积分数相同
D.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 molL﹣1<c(A)<1.56 molL﹣1
【答案】D
【解析】
试题分析:由图像可知平衡时,甲容器平衡时,A的转化率为![]() ×100%=61%,乙容器内A的转化率为
×100%=61%,乙容器内A的转化率为![]() ×100%=50%,甲容器内压强比乙容器内大,增大压强向正反应移动,增大压强平衡向着体积减小的方向移动,故:1+1>X,所以x=1。A、由上述分析可知x=1,若x=2,反应前后气体体积不变,甲、乙为等效平衡,转化率相等,A错误;B、平衡常数只与温度有关系,甲、乙两容器中反应达平衡时,平衡常数K(甲)=K(乙),B错误;C、该反应为放热反应,将乙容器单独升温,平衡向吸热反应方向移动,即向逆反应方向移动,A的转化率比甲容器的转化率低,不可能使乙容器内各物质的体积分数与甲容器内的相同,C错误;D、向甲容器中再充入2molA、2molB,可以等效为原平衡状态下压强增大一倍,平衡向正反应方向移动,A转化率增大,所以平衡时甲容器中c(A)小于2倍原平衡中的c(A),平衡移动目的是降低浓度增大趋势,但不能消除浓度增大,达新平衡时浓度比原平衡大,所以平衡时甲容器中0.78mol/L<c(A)<1.56mol/L,D正确,答案选D。
×100%=50%,甲容器内压强比乙容器内大,增大压强向正反应移动,增大压强平衡向着体积减小的方向移动,故:1+1>X,所以x=1。A、由上述分析可知x=1,若x=2,反应前后气体体积不变,甲、乙为等效平衡,转化率相等,A错误;B、平衡常数只与温度有关系,甲、乙两容器中反应达平衡时,平衡常数K(甲)=K(乙),B错误;C、该反应为放热反应,将乙容器单独升温,平衡向吸热反应方向移动,即向逆反应方向移动,A的转化率比甲容器的转化率低,不可能使乙容器内各物质的体积分数与甲容器内的相同,C错误;D、向甲容器中再充入2molA、2molB,可以等效为原平衡状态下压强增大一倍,平衡向正反应方向移动,A转化率增大,所以平衡时甲容器中c(A)小于2倍原平衡中的c(A),平衡移动目的是降低浓度增大趋势,但不能消除浓度增大,达新平衡时浓度比原平衡大,所以平衡时甲容器中0.78mol/L<c(A)<1.56mol/L,D正确,答案选D。

练习册系列答案
相关题目