题目内容
【题目】分析城市空气样本,主要污染物为可吸入颗粒物pm2.5、NOx、SO2等,其主要来源为燃煤和机动车尾气排放等。
(1) 某同学为检测样本中所含成份,将样本用蒸馏水处理制成待测试样,设计实验及实验现象如下:
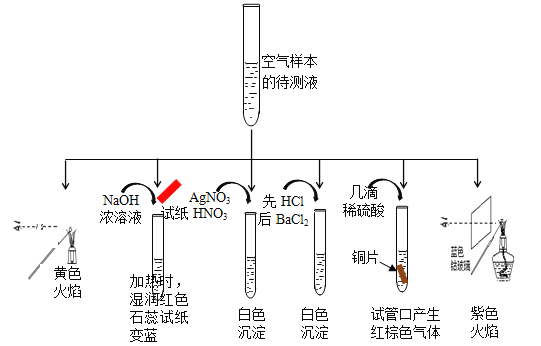
①该实验能确认存在的阳离子是 。
②该实验检测出样本中有NO3-,根据是(用化学方程式解释) 。
③根据该实验能否确定样本中含有SO32-, (填“能”或“否”) ,若要确定SO32-,所需的实验药品可以是 。
(2)PM2.5是指大气中直径小于或等于2.5μm(1μm =103 nm)的颗粒物。下列说法不正确的是 (填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1 ~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(3)科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2。
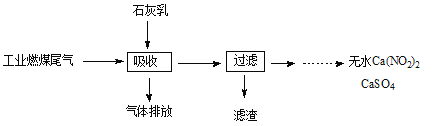
①CaSO4可以调节水泥的硬化时间。尾气中SO2与石灰乳反应生成CaSO4的化学方程式为 。
②Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式 。
【答案】(1)①Na+、NH4+、K+
②3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O(1分)2NO+O2=2NO2(1分)
③否;酸性高锰酸钾溶液(各1分,共2分)
(2)bc(2分,漏选1分\错选不得分)
(3)①2SO2+O2+2Ca(OH)2=2CaSO4+2H2O(2分)
②NO+NO2+Ca(OH)2=Ca(NO2)2+H2O(2分)
【解析】
试题分析:(1)①物质焰色反应为黄色,所以含有钠离子,和强碱共热反应产生氨气,能使石蕊试纸变蓝,证明含有铵根离子,加入硝酸酸化的硝酸银会产生白色沉淀,证明含有氯离子或是亚硫酸根离子中的一种,先加盐酸再加入氯化钡,产生白色沉淀,证明含有硫酸根离子,溶液中加入几滴硫酸,再加入金属铜,可以产生红棕色的气体,证明原溶液含有硝酸根离子,透过钴玻璃观察焰色反应呈现紫色,证明含钾离子,一定含有的钾离子是Na+、NH4+、K+;
②溶液中加入几滴硫酸,再加入金属铜,可以产生红棕色的气体,证明原溶液含有硝酸根离子,金属铜可以和硝酸反应产生硝酸铜、一氧化氮和水,一氧化氮遇到空气迅速变为红棕色,即:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2;
③该实验不能确定样本中含有SO32-,加入硝酸酸化的硝酸银会产生白色沉淀,证明可能含有氯离子或是亚硫酸根离子中的一种,亚硫酸根离子可以和硝酸之间反应得到硫酸根离子,亚硫酸根离子可以使高锰酸钾褪色,但是硫酸根离子不能,可以采用高锰酸钾检验亚硫酸根离子的存在;
(2)a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程,a正确;b.PM2.5颗粒小,但仍然对人体有害,b错误;c.直径介于1~2.5μm的颗粒物分散到空气中不能形成胶体,应该是1nm~100nm,c错误;d.推广使用电动汽车,可以减少PM2.5的污染,d正确,答案选bc;
(3)①尾气中SO2与石灰乳反应生成CaSO4,说明还有氧气参与,反应化学方程式为2SO2 + O2 +2Ca(OH)2=2CaSO4 + 2H2O。②NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式为NO + NO2 + Ca(OH)2=Ca(NO2)2 + H2O。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案