题目内容
[化学一选修3:物质结构与性质]
一水硫酸四氨合铜(Ⅱ)(化学式为[Cu(NH3)4SO4?H2O]是一种重要的染料及农药中间体.某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下图:

请回答:
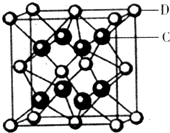
(1)沉淀A的晶体中最小环上的原子个数为 ,气体C分子中σ键和π键的个数比为 .
2)溶液D的溶质阴离子的空间构型为 ,其中心原子的杂化轨道类型为 .
3)MgO的熔点高于CuO的原因为 .
4)画出一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)的配位键 .
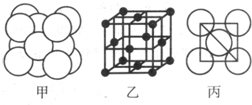
(5)湿法炼铜就是利用溶液D制得铜单质,铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示.
①铜单质晶体中原子的堆积方式为 ,晶胞中Cu原子的配位数为 .
若Cu原子半径为acm,则Cu单质晶体的密度为 g/cm3(只列出计算式,阿伏加德罗常数的值为NA).
一水硫酸四氨合铜(Ⅱ)(化学式为[Cu(NH3)4SO4?H2O]是一种重要的染料及农药中间体.某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下图:

请回答:
(1)沉淀A的晶体中最小环上的原子个数为
2)溶液D的溶质阴离子的空间构型为
3)MgO的熔点高于CuO的原因为
4)画出一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)的配位键
(5)湿法炼铜就是利用溶液D制得铜单质,铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示.

①铜单质晶体中原子的堆积方式为
若Cu原子半径为acm,则Cu单质晶体的密度为
分析:孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SiO2杂质)和稀硫酸反应生成硫酸铜、二氧化碳、硫酸铁,二氧化硅不溶于稀硫酸,所以A是二氧化硅,B中含有硫酸铁、硫酸铜,C是二氧化碳,B中加入氧化铜调节溶液的pH生成氢氧化铁,则溶液中存在硫酸铜.
(1)在二氧化硅晶体结构中,每个硅原子结合4个氧原子,同时每个氧原子结合2个硅原子;二氧化碳分子中含有2个σ键和2个π键;
(2)溶液D的溶质阴离子为硫酸根离子,根据价层电子对互斥理论确定其空间构型和中心原子杂化方式;
(3)离子晶体的熔点与晶格能成正比,晶格能与电荷成正比,与离子半径成反比;
(4)一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)中铜原子和氮原子形成4个配位键;
(5)①该类型为面心立方最密堆积;配位数=3×8×
=12;
②根据ρ=
计算.
(1)在二氧化硅晶体结构中,每个硅原子结合4个氧原子,同时每个氧原子结合2个硅原子;二氧化碳分子中含有2个σ键和2个π键;
(2)溶液D的溶质阴离子为硫酸根离子,根据价层电子对互斥理论确定其空间构型和中心原子杂化方式;
(3)离子晶体的熔点与晶格能成正比,晶格能与电荷成正比,与离子半径成反比;
(4)一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)中铜原子和氮原子形成4个配位键;
(5)①该类型为面心立方最密堆积;配位数=3×8×
| 1 |
| 2 |
②根据ρ=
| m |
| V |
解答:解:孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SiO2杂质)和稀硫酸反应生成硫酸铜、二氧化碳、硫酸铁,二氧化硅不溶于稀硫酸,所以A是二氧化硅,B中含有硫酸铁、硫酸铜,C是二氧化碳,B中加入氧化铜调节溶液的pH生成氢氧化铁,则溶液中存在硫酸铜,
(1)二氧化硅晶体结构中,每个硅原子结合4个氧原子原子,同时每个氧原子结合2个硅原子原子,最小的环上,有6个Si原子和6个O原子,所以一共12个原子;二氧化碳分子中含有2个σ键和2个π键,所以σ键和π键个数比为1:1,
故答案为:12;1:1;
(2)溶液D的溶质阴离子为硫酸根离子,SO42-中价层电子对个数,4+
(6+2-4×2)=4,所以为正四面体结构,中心原子采用 sp3 杂化,
故答案为:正四面体;sp3;
(3)离子晶体的熔点与晶格能成正比,晶格能与电荷成正比,与离子半径成反比,氧化镁的中镁离子直径小于铜离子,所以氧化镁的晶格能大于氧化铜,则氧化镁的熔点高,
故答案为:MgO的晶格能大;
(4)一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)中铜原子和氮原子形成4个配位键,其配位键表示为 ,
,
故答案为: ;
;
(5)①根据图片知,铜单质为面心立方最密堆积,铜原子配位数=3×8×
=12,
故答案为:面心立方最密堆积;12;
③Cu原子半径为acm,则晶胞边长=2
acm,晶胞体积V=(2
acm)3,每个晶胞中铜原子个数=8×
+6×
=4ρ=
=
=
g/cm3=
g/cm3,
故答案为:
.
(1)二氧化硅晶体结构中,每个硅原子结合4个氧原子原子,同时每个氧原子结合2个硅原子原子,最小的环上,有6个Si原子和6个O原子,所以一共12个原子;二氧化碳分子中含有2个σ键和2个π键,所以σ键和π键个数比为1:1,
故答案为:12;1:1;
(2)溶液D的溶质阴离子为硫酸根离子,SO42-中价层电子对个数,4+
| 1 |
| 2 |
故答案为:正四面体;sp3;
(3)离子晶体的熔点与晶格能成正比,晶格能与电荷成正比,与离子半径成反比,氧化镁的中镁离子直径小于铜离子,所以氧化镁的晶格能大于氧化铜,则氧化镁的熔点高,
故答案为:MgO的晶格能大;
(4)一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)中铜原子和氮原子形成4个配位键,其配位键表示为
 ,
,故答案为:
 ;
;(5)①根据图片知,铜单质为面心立方最密堆积,铜原子配位数=3×8×
| 1 |
| 2 |
故答案为:面心立方最密堆积;12;
③Cu原子半径为acm,则晶胞边长=2
| 2 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
| ||
| V |
| ||
(2
|
| 64×4 | ||
(2
|
故答案为:
| 64×4 | ||
(2
|
点评:本题考查较综合,涉及晶胞的计算、配位键、杂化方式的判断、离子空间构型的判断等知识点,根据价层电子对互斥理论确定杂化方式和离子空间构型,难点是晶胞的计算,注意晶胞的边长不是铜原子直径,为易错点.

练习册系列答案
相关题目
 或
或
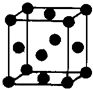 (2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表:
(2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表: