题目内容
【题目】50mL浓硫酸和铜片加热后反应,铜片完全溶解后测得产生4.48L(标况下)气体,把反应后的溶液稀释至1L,取20mL溶液加入足量BaCl2溶液产生3.262g沉淀,求原硫酸溶液的物质的量浓度是多少______?
【答案】18mol/L
【解析】
硫酸中S元素一部分变为SO2,一部分仍以SO42-形成存在溶液中,先计算SO2、剩余SO42-的物质的量,然后根据c=![]() 计算原硫酸的物质的量浓度。
计算原硫酸的物质的量浓度。
Cu与浓硫酸发生反应:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,反应产生的SO2的物质的量为n(SO2)=
CuSO4+SO2↑+2H2O,反应产生的SO2的物质的量为n(SO2)=![]() =
=![]() =0.2mol,反应后溶液中硫酸铜及未反应的硫酸电离产生的SO42-与加入的BaCl2溶液发生离子反应:Ba2++ SO42-=BaSO4↓,在1L反应后溶液中含有的SO42-的物质的量为n(SO42-)=
=0.2mol,反应后溶液中硫酸铜及未反应的硫酸电离产生的SO42-与加入的BaCl2溶液发生离子反应:Ba2++ SO42-=BaSO4↓,在1L反应后溶液中含有的SO42-的物质的量为n(SO42-)=![]() =0.7mol,则根据S元素守恒,可知原浓硫酸中含有硫酸的物质的量为n(H2SO4)=n(SO42-)+n(SO2)=0.7mol+0.2mol=0.9mol,所以c(H2SO4)=
=0.7mol,则根据S元素守恒,可知原浓硫酸中含有硫酸的物质的量为n(H2SO4)=n(SO42-)+n(SO2)=0.7mol+0.2mol=0.9mol,所以c(H2SO4)=![]() =18mol/L。
=18mol/L。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
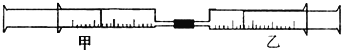
实验序号 | 甲针筒内物质 | 乙针筒内物质 |
1 | 溴水 | SO2 |
2 | H2S | SO2 |
3 | NO2(主要) | H2O(l) |
4 | 15mLCl2 | 40mLNH3 |
试回答下列问题:
(1)实验1中,溶液颜色由______色变为______色,写出溶液变色的化学反应方程式____________。
(2)实验2甲针筒内发生的化学反应方程式:_______________。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入________溶液中。
(3)实验3中,甲中最后剩余的无色气体是_____,写出NO2与H2O反应的化学反应方程式_____________。
(4)实验4中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式______________,写出检验所得白色固体中阳离子的操作方法:___________。