题目内容
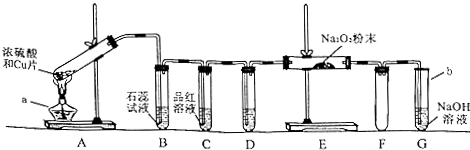
(1)SO2是一种________色、有________气味的有毒气体,密度比空气________,容易液化,易溶于水(1∶40).
(2)SO2的化学性质丰富多彩.SO2是一种________氧化物,可以与水、碱、碱性氧化物反应.由于SO2分子中硫元素的化合价为+4,处于S的中间价态,所以SO2既可作还原剂(主要),也可作氧化剂(次要).当SO2遇到强氧化剂时,+4价的S可以被氧化为+6价的S,SO2作为还原剂.例如,SO2能与O2反应生成SO3(写出相应的化学方程式,下同):________;SO2还能使溴水褪色:________.当SO2遇到强还原剂时,+4价的S可以被还原为0价的S,SO2作为氧化剂.例如,SO2可以与H2S反应生成单质硫:________.除此之外,SO2能使________褪色,这是因为SO2具有漂白性,能与有色物质化合生成不稳定的无色化合物.
答案:

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目