题目内容
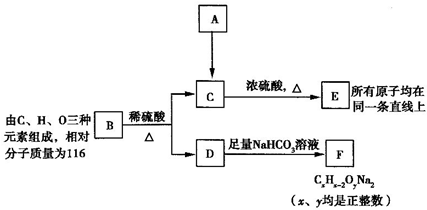
铜在浓硫酸中加热能发生如下反应:Cu+2H2SO4
CuSO4+SO2↑+2H2O.某化学兴趣小组的同学设计了如图所示实验,准备探究铜与浓硫酸反应的情况及生成物的性质.请你也一起进行探究,并完成以下的问题.

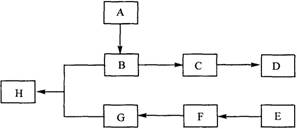
(1)图中标号的仪器名称分别为:a
(2)对实验开始后各装置出现的现象描述及判断:
①当A中观察到铜片溶解、有气泡生成时,还能观察到溶液变
②B中的石蕊试液若变
③C中品红溶液由红色变成无色,说明生成物中的SO2具有
(3)C中逸出的SO2气体经装置D中盛装的
(4)F装置的作用是:
| ||

(1)图中标号的仪器名称分别为:a
酒精灯
酒精灯
,b试管
试管
.(2)对实验开始后各装置出现的现象描述及判断:
①当A中观察到铜片溶解、有气泡生成时,还能观察到溶液变
蓝
蓝
色的现象;②B中的石蕊试液若变
红
红
色,说明生成物中的SO2是一种酸性的气体;③C中品红溶液由红色变成无色,说明生成物中的SO2具有
漂白
漂白
性.(3)C中逸出的SO2气体经装置D中盛装的
浓硫酸
浓硫酸
溶液干燥后通入装置E,用带火星的木条伸进G中,木条能复燃,说明E中的反应有氧气
氧气
生成;E中反应的化学方程式是:2Na2O2+2SO2=2Na2SO3+O2
2Na2O2+2SO2=2Na2SO3+O2
.(4)F装置的作用是:
防止发生倒吸时G中溶液进入装置E中
防止发生倒吸时G中溶液进入装置E中
.分析:(1)依据装置图分析仪器名称;
(2)①浓硫酸和铜加热反应生成硫酸铜溶液呈蓝色;
②铜和浓硫酸反应生成二氧化硫气体通入石蕊试液中二氧化硫和水反应生成亚硫酸具有酸性;
③二氧化硫具有漂白性;
(3)C中逸出的SO2气体经装置D中的浓硫酸干燥后通过装置E,生成了使带火星的木条复燃的气体为氧气,依据二氧化碳和过氧化钠反应类比得到;
(4)分析F装置是防倒吸的作用.
(2)①浓硫酸和铜加热反应生成硫酸铜溶液呈蓝色;
②铜和浓硫酸反应生成二氧化硫气体通入石蕊试液中二氧化硫和水反应生成亚硫酸具有酸性;
③二氧化硫具有漂白性;
(3)C中逸出的SO2气体经装置D中的浓硫酸干燥后通过装置E,生成了使带火星的木条复燃的气体为氧气,依据二氧化碳和过氧化钠反应类比得到;
(4)分析F装置是防倒吸的作用.
解答:解:(1)装置图分析可知a为酒精灯,b为试管,
故答案为:酒精灯,试管;
(2)①浓硫酸和铜加热反应生成硫酸铜溶液呈蓝色,当A中观察到铜片溶解、有气泡生成时,还能观察到溶液变蓝,
故答案为:蓝;
②铜和浓硫酸反应生成二氧化硫气体通入石蕊试液中二氧化硫和水反应生成亚硫酸具有酸性,使石蕊试液变红色,说明二氧化硫是酸性气体,
故答案为:红;
③二氧化硫具有漂白性,通过品红试液能使试液褪色,
故答案为:漂白;
(3)C中逸出的SO2气体经装置D中的浓硫酸干燥后通过装置E,生成了使带火星的木条复燃的气体为氧气,依据二氧化碳和过氧化钠反应的产物,分析写出二氧化硫和过氧化钠反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2,
故答案为:浓硫酸,氧气;2Na2O2+2SO2=2Na2SO3+O2;
(4)F装置是安全装置,可以防止G中溶液倒吸到E装置炸裂玻璃管,
故答案为:防止发生倒吸时G中溶液进入装置E中.
故答案为:酒精灯,试管;
(2)①浓硫酸和铜加热反应生成硫酸铜溶液呈蓝色,当A中观察到铜片溶解、有气泡生成时,还能观察到溶液变蓝,
故答案为:蓝;
②铜和浓硫酸反应生成二氧化硫气体通入石蕊试液中二氧化硫和水反应生成亚硫酸具有酸性,使石蕊试液变红色,说明二氧化硫是酸性气体,
故答案为:红;
③二氧化硫具有漂白性,通过品红试液能使试液褪色,
故答案为:漂白;
(3)C中逸出的SO2气体经装置D中的浓硫酸干燥后通过装置E,生成了使带火星的木条复燃的气体为氧气,依据二氧化碳和过氧化钠反应的产物,分析写出二氧化硫和过氧化钠反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2,
故答案为:浓硫酸,氧气;2Na2O2+2SO2=2Na2SO3+O2;
(4)F装置是安全装置,可以防止G中溶液倒吸到E装置炸裂玻璃管,
故答案为:防止发生倒吸时G中溶液进入装置E中.
点评:本题考查了浓硫酸性质的分析判断,产物性质的实验验证实验方法和反应现象应用,主要是二氧化硫性质的分析应用,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目