题目内容
4.下列离子方程式正确的是( )| A. | 1mol Cl2通入含1molFeBr2的溶液中 $C{l_2}+F{e^{2+}}+2B{r^-}=F{e^{3+}}+B{r_2}+2C{l^-}$ | |
| B. | 用大理石跟稀盐酸制二氧化碳:CO32-+2H+=H2O+CO2↑ | |
| C. | 碳酸氢钠溶液中加入过量澄清石灰水:2HCO3-+Ca2++2OH-=CO32-+CaCO3↓+2H2O | |
| D. | 氧化镁与盐酸混合:MgO+2H+=Mg2++H2O |
分析 A.由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化;
B.碳酸钙在离子反应中保留化学式;
C.反应生成碳酸钙、水、NaOH;
D.反应生成氯化镁和水.
解答 解:A.1mol Cl2通入含1molFeBr2的溶液中的离子反应为2Fe2++2Cl2+2Br-═2Fe3++4Cl-+Br2,故A错误;
B.用大理石跟稀盐酸制二氧化碳的离子反应为CaCO3+2H+=H2O+CO2↑+Ca2+,故B错误;
C.碳酸氢钠溶液中加入过量澄清石灰水的离子反应为HCO3-+Ca2++OH-=CaCO3↓+H2O,故C错误;
D.氧化镁与盐酸混合的离子反应为MgO+2H+=Mg2++H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应的考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
14.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 在常温常压下,11.2L氯气含有的分子数为0.5NA | |
| B. | 在常温常压下,1mol氦气含有的原子数为NA | |
| C. | 32g氧气含有的原子数目为NA | |
| D. | 标准状况下,1L乙烷完全燃烧后,所生成的气态产物的分子数为6NA/22.4 |
15.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是( )
| A. | 油脂都是高级饱和脂肪酸甘油酯,不能使溴的四氯化碳溶液褪色 | |
| B. | 糖类、脂肪和蛋白质都能发生水解反应 | |
| C. | 蔗糖和麦芽糖互为同分异构体,可以利用银氨溶液区别二者 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
19.下列物质的溶液在空气中放置一段时间,溶液的pH值会有下降现象的是(不考虑溶质挥发)( )
①H2S;②H2SO3;③浓H2SO4;④Na2CO3;⑤氯水;⑥Ca(OH)2;⑦Na2SO3.
①H2S;②H2SO3;③浓H2SO4;④Na2CO3;⑤氯水;⑥Ca(OH)2;⑦Na2SO3.
| A. | ②③⑤⑥⑦ | B. | ①②④⑤⑥ | C. | ②⑥⑦ | D. | ③④⑤⑦ |
9.下列物质在水中的电离方程式书写正确的是( )
| A. | NaHSO4═Na++HSO4- | B. | NaHCO3═Na++H++CO32- | ||
| C. | KClO3═K++Cl-+3O2- | D. | Al2(SO4)3═2Al3++3SO42- |
16.下列说法不正确的是( )
| A. | 标准状况下,气体摩尔体积约为22.4 L/mol | |
| B. | 非标准状况下,1mol任何气体都不可能为22.4L | |
| C. | 标准状况下,22.4L任何气体的物质的量都约为1mol | |
| D. | 标准状况下,1 molH2O的体积小于22.4L |
7.下列各组物质互为同分异构体的是( )
| A. | CH4和CH3-CH2-CH3 | B. | C2H5-OH和C6H5-OH | ||
| C. | CH3-CH2-CH2-CH3和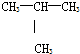 | D. | C2H4和C3H4 |
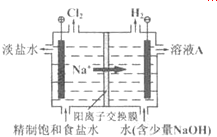 生产生活中广泛涉及氧化还原反应.
生产生活中广泛涉及氧化还原反应.