题目内容
1.下列物质既能与氢氧化钠溶液又能与盐酸反应的是( )| A. | NH4Cl | B. | Mg(OH)2 | C. | Al2O3 | D. | Fe2O3 |
分析 Al、Al2O3、Al(OH)3、弱酸酸式盐、弱酸铵盐、氨基酸、蛋白质等物质都能和稀盐酸、NaOH反应,据此分析解答.
解答 解:A.氯化铵是强酸弱碱盐,只能和NaOH反应不能和稀盐酸反应,故A错误;
B.氢氧化镁属于碱,只能和稀盐酸反应,不和氢氧化钠反应,故B错误;
C.氧化铝是两性氧化物,能和氢氧化钠、稀盐酸反应生成盐和水,故C正确;
D.氧化铁属于碱性氧化物,只能和稀盐酸反应生成氯化铁和水,故D错误;
故选C.
点评 本题考查元素化合物性质,为高频考点,明确铝及其化合物性质的特殊性,注意氧化铝、氢氧化铝能和强碱反应但和弱碱不反应,为易错点.

练习册系列答案
相关题目
11.下列实验操作中有错误的是( )
| A. | 蒸馏操作时,应使温度计水银球置于混合液中 | |
| B. | 蒸馏操作时,冷却水应从冷凝管的下口通入,上口流出 | |
| C. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热 |
12.以下4种有机物的分子式都是C4H10O:①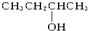 ②
②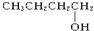 ③
③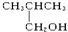 ④
④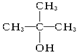 其中能被氧化为含相同碳原子数的醛的是( )
其中能被氧化为含相同碳原子数的醛的是( )
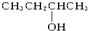 ②
②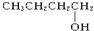 ③
③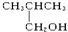 ④
④ 其中能被氧化为含相同碳原子数的醛的是( )
其中能被氧化为含相同碳原子数的醛的是( )| A. | ①② | B. | 只有② | C. | ③④ | D. | ②③ |
9.现有H2O、NH3、CH4三种物质,它们分别都含有等物质的量的氢原子,则三种物质的物质的量之比为( )
| A. | 1:1:1 | B. | 6:3:2 | C. | 4:3:2 | D. | 6:4:3 |
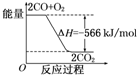
13.根据热化学方程S (s)+O2(g)═SO2 (g)△H=-297.23kJ/mol (反应在298K,101kPa下发生)分析下列说法正确的是( )
| A. | 标况下,燃烧1mol S吸收的热量为297.23 kJ | |
| B. | S (g)+O2 (g)═SO2 (g) 放出的热量大于297.23 kJ | |
| C. | S (g)+O2 (g)═SO2 (g)放出的热量小于297.23 kJ | |
| D. | 形成1 mol SO2 的化学键所释放的总能量大于断裂 1 molS (s)和 1mol O2 (g)的化学键所吸收的总能量 |
 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、S、NOX等进行研究具有重要意义.为减少SO2的排放,常采取的措施是:将煤转化为清洁气体燃料.涉及的化学反应为:
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、S、NOX等进行研究具有重要意义.为减少SO2的排放,常采取的措施是:将煤转化为清洁气体燃料.涉及的化学反应为: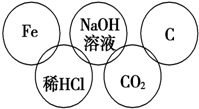 小美在五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应.请完成下列问题:
小美在五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应.请完成下列问题: