题目内容
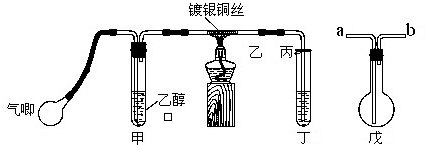
某课外活动小组利用如图所示装置分别做如下实验:
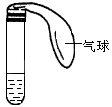 ①在试管中注入某红色溶液,加热试管,溶液颜色变浅,冷却后
①在试管中注入某红色溶液,加热试管,溶液颜色变浅,冷却后
恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:_________________________。②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色, 则此溶液可能是_____________溶液;加热时溶液由无色变为红色的原因是:__________________________________。
①滴有酚酞的氨水,加热时溶液中的NH3·H2O分解逸出氨气,溶液碱性减弱。②被SO2漂白的品红溶液,加热时分解出SO2气体。
解析:
本题能力层次为C。氨水呈碱性,加热时由于氨气挥发,溶液碱性减弱;二氧化硫使品红溶液褪色,加热使无色物质分解出二氧化硫而颜色又变红色。
学法指导:氨水呈碱性: NH3+H2O![]() NH3·H2O NH3·H2O
NH3·H2O NH3·H2O![]() NH4++OH-
NH4++OH-
加热时NH3·H2O分解,溶液中的氨气逸出: NH3·H2O![]() NH3↑+ H2O。
NH3↑+ H2O。
SO2的漂白性和Cl2的漂白性的主要区别是①原理不同。Cl2的漂白性是因为Cl2和H2O反应产生HClO的强氧化性将色素氧化,而SO2和色素化合生成一种不稳定的无色物质;②强弱程度不同。Cl2的漂白性比SO2的漂白性强些,如Cl2通入石蕊溶液中可以看到先变红后褪色,SO2通入石蕊溶液中,看到只变红不褪色;③Cl2漂白的物质不会恢复原来颜色,SO2漂白的物质时间长了或加热时可以恢复原来颜色。

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案
相关题目
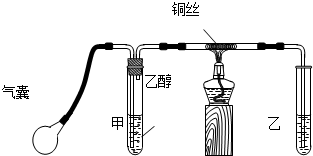
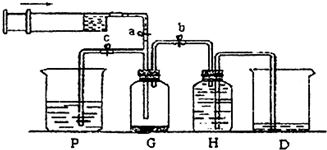
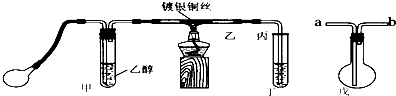 某课外活动小组利用如图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置己略去,粗黑线表示乳胶管.请填写下列空白:
某课外活动小组利用如图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置己略去,粗黑线表示乳胶管.请填写下列空白: