题目内容
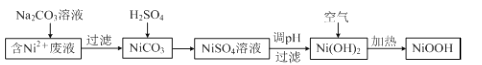
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验:

已知:3NO3-+8Al+5OH-+2H2O![]() 3NH3↑+8AlO2-
3NH3↑+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A.试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B.试样中一定不含Al3+
C.试样中可能存在Na+、Cl-
D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4
【答案】B
【解析】
试题分析:试样溶液中加入过量Ba(OH)2并加热,生成的气体1,该气体1可能是NH3,则试样中含有NH4+;向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,NO3-+A1+OH-+H2O→NH3↑+[Al(OH)4]-,生成气体2,该气体是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg2+。A.根据以上分析可知溶液中含有NH4+、Mg2+、SO42-和NO3-,故A正确;B.根据实验操作不能确定是否含有Al3+,即试样中可能含有Al3+,故B错误;C.根据实验无法确定是否含有Na+、Cl-,所以溶液中可能含有Na+、Cl-,故C正确;D.根据以上分析可知溶液中含有NH4+、Mg2+、SO42-和NO3-,则该雾C中可能存在NaNO3、NH4Cl和MgSO4,故D正确;故选B。

 阅读快车系列答案
阅读快车系列答案【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A | 乙酸具有酸性 | 常用于除水垢 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
【题目】电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
化学式 | 电离平衡常数 |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为________________________________。(填写序号)
(2)25 ℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为______ ___。
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是 。
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-)
D.c(HCN)+ c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理_____________________。
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小___________________;电荷守恒表达式 ___________________ 。
(6)H2C2O4溶液和KMnO4酸性溶液可发生反应:H2C2O4+MnO4-+H+→CO2+Mn2++H2O,反应中每生成标况下4.48LCO2气体,转移的电子的物质的量为__________mol。