题目内容
【题目】石蜡油分解可产生乙烯。乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的主要化学性质,实验装置如图所示。
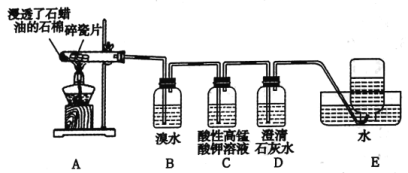
(1)用化学反应方程式解释B装置中的实验现象:_________。
(2)C装置中的现象是_________,其发生反应的类型是__________。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_______(填序号)中的实验现象可判断该资料是否真实。
【答案】![]() 酸性高锰酸钾溶液褪色 氧化反应 D
酸性高锰酸钾溶液褪色 氧化反应 D
【解析】
(1)B装置中乙烯与溴发生加成反应;
(2)乙烯具有还原性,C装置中乙烯与酸性高锰酸钾溶液发生氧化反应;
(3)二氧化碳能使澄清石灰水变浑浊;
(1)乙烯含有碳碳双键, 能够与溴发生加成反应而使溴水褪色,反应方程式为![]() ;
;
(2)乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化反应而使酸性高锰酸钾溶液褪色;
(3)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,根据D装置中石灰水是否变浑浊判断资料的真实性。

 阅读快车系列答案
阅读快车系列答案【题目】常温时,已知部分弱酸的电离平衡常数如下表:
弱酸 | CH3COOH | H2S | H2CO3 | H2SO3 |
电离平衡常数(25 ℃) | K=10-5 | K1=1.3×10 -7 K2=7.1×10 -15 | K1=4.4×10 -7 K2=4.7×10 -11 | K1=1.3×10 -2 K2=6.3×10 -8 |
请回答下列问题:
(1)H2S 的第二级电离平衡常数的表达式 K2=______
(2)25℃时,若 CH3COOH 的起始浓度为 0.1 mol·L -1,则平衡时 c(H+)=____mol/L,由水电离的出的 c(H+)=____mol/L。
(3)(A)相同浓度的①CH3COONa 溶液、②Na2CO3溶液、③Na2S溶液、④NaHSO3溶液和⑤Na2SO3溶液,pH 由大到小排序为________(用序号表示)
(B)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)___________
(4)pH 均为 5硫酸和醋酸两份溶液,把硫酸溶液稀释 1000 倍,则 c(H+)/c(SO42-)=___;把醋酸稀释 100 倍,pH 范围为_____
(5)将少量H2S气体通入到 Na2CO3溶液中发生反应的离子方程式为______
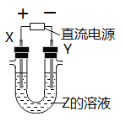
【题目】下列各组物质中,气体X和气体Y同时通入盛有溶液Z的洗气瓶中(如图),一定没有沉淀生成的是( )

X | Y | Z | |
A | NO2 | SO2 | BaCl2 |
B | NH3 | O2 | Al2(SO4)3 |
C | NH3 | CO2 | CaCl2 |
D | CO2 | SO2 | CaCl2 |
A. A B. B C. C D. D