题目内容
【题目】如图是一些常见含氯产品,根据情况回答下列问题。

(1)下列有关氯单质和氯水的说法正确的是________(填序号)。
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)用化学方程式表示漂白粉的漂白原理________________________ ;
(3)向FeSO4溶液中滴加氯水,溶液变为黄色,写出反应的离子方程式_____
(4)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因________________________(用离子方程式表示)。
(5)一定量铁粉与氯气充分反应后,加适量水,完全溶解后无固体剩余,此时所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的质量之比是________________________
【答案】①④ Ca(ClO)2+CO2+H2O=CaCO3+2HClO 2Fe2++Cl2=2Fe3++2Cl- Cl-+ClO-+2H+ = Cl2↑+H2O ![]() (或2:3)
(或2:3)
【解析】
(1)根据氯气和氯水的性质进行分析;
(2)石灰乳和氯气反应制备漂白粉;
(3)氯气具有氧化性,能够把亚铁离子氧化为铁离子;
(4)NaClO与HCl在酸性环境下发生氧化还原反应生成氯气;
(5)Fe与Cl2在点燃条件下生成FeCl3,将反应后的固体投于水中,Fe3+能与剩余的Fe反应生成FeCl2,反应的方程式:2Fe+3Cl2=2FeCl3,2Fe3++Fe=3Fe2+,据以上分析进行计算。
(1)①液氯为液态氯,为纯净物,氯水为氯气与水反应后的混合物,故①正确;
②氯气使湿润的红色布条褪色,其原因是氯气与水反应生成了具有漂白性的HClO,氯气本身不具有漂白性,故②错误;
③铁与氯气燃烧反应生成FeCl3,与反应物的量无关,故③错误;
④新制氯水中含有H+,能够使蓝色石蕊试纸变红,新制氯水中含有HClO,具有漂白性,能够使变红的试纸褪色,故④正确;
⑤新制氯水长期放置过程中,因HClO稳定性较差,见光或受热易发生分解生成HCl、O2,会使溶液的酸性增强,故⑤错误;
故答案为:①④;
(2)漂白粉的有效成分为Ca(ClO)2,其与空气中CO2反应生成具有漂白性的HClO,其反应方程式为:Ca(ClO)2+CO2+H2O=CaCO3 +2HClO;
故答案为:Ca(ClO)2+CO2+H2O=CaCO3 +2HClO;
(3)FeSO4中Fe2+具有还原性,氯水中Cl2具有氧化性,二者可发生反应生成黄色Fe3+,其反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)Cl-具有还原性,ClO-具有氧化性,二者可发生氧化还原反应,根据氧化还原反应化合价变化规律可知,二者发生归中反应生成Cl2,根据守恒关系配平反应离子方程式为:Cl-+ClO-+2H+ = Cl2↑+H2O;
故答案为:Cl-+ClO-+2H+ = Cl2↑+H2O;
(5)Fe与Cl2在点燃条件下生成FeCl3,将反应后的固体投于水中,Fe3+能与剩余的Fe反应生成FeCl2,设与Cl2反应的Fe的物质的量为xmol,与FeCl3反应的Fe的物质的量为ymol,则
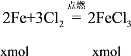
![]()
所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则1.5y=x-y,可解得x=2.5y;
已反应的Fe3+的物质的量为ymol,未反应的Fe3+的物质的量为(x-y)mol=(2.5y-y)mol=1.5ymol,因此已反应的Fe3+和未反应的Fe3+的物质的量之比为![]() =
=![]() ,其质量之比等于其物质的量之比=
,其质量之比等于其物质的量之比=![]() ;
;
故答案为:![]() (或2:3)。
(或2:3)。

【题目】下列有关实验现象和解释或结论都正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 取硫酸催化淀粉水解的反应液,滴入少量新制 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B |
| 有白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满 | 红棕色变深 | 反应 |
D | 向 | 得到红褐色透明液体 | 得到 |
A.AB.BC.CD.D