题目内容
【题目】X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系: ![]()
(1)若该反应是非氧化还原反应 ①X为强碱溶液,W是形成酸雨的主要气体,则Y到Z的离子方程式为
②X是一种盐,焰色反应为黄色,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Y的化学式为 .
③若W为一种强碱,Y具有两性,则向Z溶液中通入少量二氧化碳的离子方程式为 .
(2)若该反应是氧化还原反应 ①X常温下为黄绿色气体,W是生活中应用最广泛的金属之一,则Y的水溶液中加入W生成Z溶液的离子方程式为 .
②X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法 , X转化为Y的化学方程式为 .
【答案】
(1)SO32﹣+SO2+H2O=2HSO3﹣;NaHCO3;2AlO2﹣+CO2+3H2O=2Al(OH)3+CO32﹣
(2)2Fe3++Fe=3Fe2+;湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟;4NH3+5O2 ![]() ?4NO+6H2O
?4NO+6H2O
【解析】解:(1)①X为强碱溶液,W是形成酸雨的主要气体,W为SO2 , Y、Z分别含有SO32﹣、HSO3﹣ , 则Y到Z的离子方程式为:SO32﹣+SO2+H2O=2HSO3﹣ , 所以答案是:SO32﹣+SO2+H2O=2HSO3﹣;②X是一种盐,焰色反应为黄色,则X为钠盐,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Z为CO2 , 则X为Na2CO3 , Y为NaHCO3 , W为酸.所以答案是:NaHCO3;③若W为一种强碱,Y具有两性,则X为铝盐,Y为Al(OH)3 , Z为偏铝酸盐,向Z溶液中通入少量二氧化碳的离子方程式为:2AlO2﹣+CO2+3H2O=2Al(OH)3+CO32﹣ , 所以答案是:2AlO2﹣+CO2+3H2O=2Al(OH)3+CO32﹣;(2)①X常温下为黄绿色气体,则X为Cl2 , W是生活中应用最广泛的金属之一,由转化关系可知应为变价金属,则W为Fe,Y为FeCl3、Z为FeCl2 , Y的水溶液中加入W生成Z溶液的离子方程式为:2Fe3++Fe=3Fe2+ , 所以答案是:2Fe3++Fe=3Fe2+;②X常温下为气体化合物,Z是一种红棕色气体,则Z为NO2 , X为NH3 , W为O2 , Y为NO,NH3的检验方法:湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟,NH3转化为NO的化学方程式为:4NH3+5O2 ![]() 4NO+6H2O,所以答案是:湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟;4NH3+5O2
4NO+6H2O,所以答案是:湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟;4NH3+5O2 ![]() 4NO+6H2O.
4NO+6H2O.

 考前必练系列答案
考前必练系列答案【题目】无水四氯化锡(SnCl4) 实验室可用熔融的锡(熔点为23.9℃)与Cl2反应制备SnCl4,装置如下图所示回答下列问题:

已知SnCl4在湿空气中极易水解生成SnO2·xH2O。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
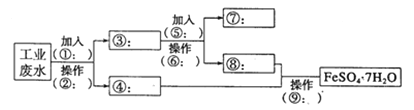
(1)a管的作用是________,装置A中发生反应的化学方程式是______________。
(2)装置B、C、F、G中盛放的最佳试剂依次为____________(填序号,试剂可重复使用)。
①饱和Na2CO3溶液 ②NaOH溶液 ③浓H2SO4 ④饱和NaCl溶液 ⑤H2O
(3)点燃酒精灯前需要进行的一步操作是______________。
(4)若撒去装置C,则装置D中可能会发生的主要副反应的化学方程式为___________。
(5)得到的产物中常混有SnCl2,某实验小组用碘氧化法滴定分析产品中SnCl4的含量(Sn2++I2=Sn4++2I-)。准确称取mg产品于锥形瓶中,用少量浓盐酸溶解,再加水稀释,淀粉溶液作指示剂,用0.1mol/L碘标准溶液滴定至终点,达到滴定终点时的现象为________,消耗碘标准溶液20.00mL,计算产品中SnCl4的含量______(用含m的代数式表示)。
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电于云均呈球形 |
Y | 原子的能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原于核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原于的围电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题:
(1)基态T2+的电子排布式为____________。
(2)Y.Z.R 的电负性由大到小的顺序为____________ (用元素符号表示)。
(3)YX4+的空间构型为____________,离子中Y原子的杂化轨道类型为____________ ,YX4+电子式为________。
(4)YX3的一种等电子体分子是______,YX3 的键角大于X2Z的键角的主要原因是________。
(5)T单质不溶于YX3溶液,也不溶于X2Z溶液,但能溶于它们的混合溶液,其主要原因是形成了稳定的[T(YX3)4]2+,1mol该阳离子中共含有______mol σ键。
(6)Z、T组成的晶胞结构如下图所示。已知Z、T原子的半径分别为apm、bpm,晶胞边长为cpm,则该晶胞中原子的空间利用率为________(用代数式表示)。