题目内容
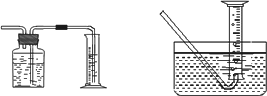
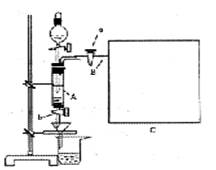
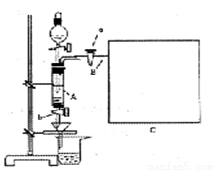
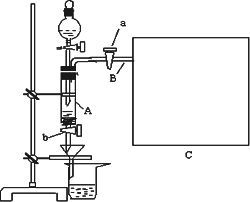
三氯化铁是中学化学实验室中必不可少的重要试剂.某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3·6H2O,该同学设计的实验装置如图所示,A中放有m克废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,从分液漏斗内向A中加过量的稀盐酸,充分反应后溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使多余HNO3挥发,再降温结晶得FeCl3·6H2O晶体.填写下列空白:
(1)滴加盐酸,发现反应速率比同浓度盐酸与纯铁粉反应要快,其原因是________;
(2)将烧杯内溶液用蒸发、浓缩、再降温结晶法制得FeCl3·6H2O晶体,而不用直接蒸干溶液的方法来制得晶体的理由________;
(3)用该法制得的晶体中往往混有Fe(NO3)3,为了制得较纯净的FeCl3·6H2O,可将烧杯内的稀硝酸换成________;
(4)若要求废铁屑的纯度,需要测出从B中排出气体的体积.若测得排出的气体体积为V(已折算成标准状况,单位:L),则废铁屑的纯度为________(用m、V的代数式表示);
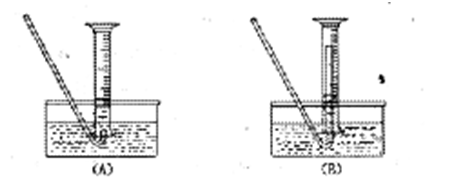
(5)为了测出从B中放出气体的体积V,请自选仪器在C处设计简便、合理的集气装置,并在上面框格中画出该装置图(假设所用仪器的体积均足够大).
答案:
解析:
解析:
|
(1)铁粉与杂质铜形成原电池反应,加快了反应速率. (2)因为氯化铁是强酸弱碱盐水解生成氢氧化铁和盐酸,加热蒸干时使HCl 挥发造成水解平衡右移,因此得不到FeCl3·6H2O晶体 (3)双氧水或新制氯水(填任一个均给满分) (4)250 V/m% (5)
(画出其一即可) |

练习册系列答案
相关题目