题目内容
【题目】下列说法正确的是
A.一定温度下,10mL 0.50mol·L-1 NH4Cl溶液与20mL 0.25mol·L-1 NH4C1溶液含NH4+物质的量相同
B.25℃时,将a mo1·L-l氨水与0.01 moI·L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3·H2O的电离常数![]()
C.一定温度下,已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液中
CH3COO-+H+,加少量烧碱溶液可使溶液中![]() 值增大。
值增大。
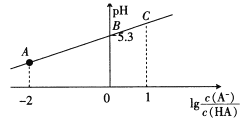
D.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB
【答案】B
【解析】
A、10mL 0.50mol·L-1 NH4Cl溶液与20mL 0.25mol·L-1 NH4C1溶液中溶质的物质的量相同。铵根离子的水解是可逆反应,铵根离子的浓度越大,水解程度越小,所以铵根离子的物质的量不相等,错误;
B、25℃时,将a mo1·L-l氨水与0.01 moI·L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),则溶液呈中性,所以氨水过量,过量的NH3·H2O的浓度为c(NH3·H2O)=![]() mol/L,c(NH4+)=c(C1-)=0.01mol/L÷2=0.005mol/L,溶液呈中性,则c(OH-)= c(H+)=10-7mol/L,所以NH3·H2O的电离常数K=
mol/L,c(NH4+)=c(C1-)=0.01mol/L÷2=0.005mol/L,溶液呈中性,则c(OH-)= c(H+)=10-7mol/L,所以NH3·H2O的电离常数K= =
= =
=![]() ,正确;
,正确;
C、向醋酸溶液中加入氢氧化钠,则氢离子浓度减小,平衡正向移动,醋酸根离子浓度增大,![]() =
=![]() ,所以比值减小,错误;
,所以比值减小,错误;
D、等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA的物质的量大,则HA的电离度小,所以HA的酸性较弱,错误。
答案选B。

【题目】中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如下图所示。

已知:几种物质中化学键的键能如下表所示。
化学键 | H2O中H—O键 | O2中O=O 键 | H2中H—H键 | H2O2中O—O键 | H2O2中O—H键 |
键能kJ/mol | 463 | 496 | 436 | 138 | 463 |
若反应过程中分解了2 mol水,则下列说法不正确的是
A. 总反应为2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B. 过程I吸收了926 kJ能量
C. 过程II放出了574 kJ能量
D. 过程Ⅲ属于放热反应
【题目】学习中经常应用类推法。下列表格左边正确,类推法应用于右边也正确的是( )
A | 向FeCl2溶液中滴入氯水 2Fe2++Cl2=2Fe3++2Cl— | 向FeCl2溶液中滴入碘水 2Fe2++I2=2Fe3++2I— |
B | 向澄清石灰水中通入少量CO2气体 Ca2++2OH—+CO2 =CaCO3↓+H2O | 向澄清石灰水中通入少量SO2 气体 Ca2++2OH—+SO2=CaSO3↓+H2O |
C | 向Na2CO3溶液中滴入稀HNO3
| 向Na2SO3溶液中滴入稀HNO3
|
D | 锌粒放入硫酸亚铁溶液中 Zn+Fe2+=Zn2++Fe | 钠投入硫酸铜溶液中 2Na+Cu2+=2Na++Cu |
A. A B. B C. C D. D
【题目】某化学课外小组用如图所示装a制取溴苯并探究该反应的类型。先向分液漏斗中加人苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。
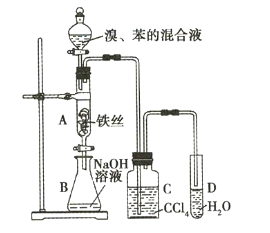
(1)反应结束后,打开A下端的活塞,让反应液流入B中,充分振荡,目的是___。
(2)C中盛放CCl4的作用是___。
(3)若要证明苯和液溴发生的是取代反应,而不是加成反应,通常有两种方法,请按要求填写下表。
向试管D中加入的试剂 | 能证明苯与液溴发生取代反应的现象 | |
方法一 | ___ | ___ |
方法二 | ___ | ___ |