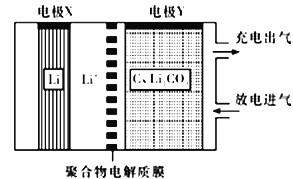
��Ŀ����
����Ŀ����ԭ�������ĵ��������ֶ�����Ԫ��(����ĸx�ȱ�ʾ)ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯����ͼ��ʾ��

�����жϳ���Ԫ�ػش�:
(1)x��Ԫ�����ڱ���λ����________________________��
(2)y������������Ӧ��ˮ���������⻯�ﷴӦ�������к��л�ѧ��������Ϊ________________��
(3)d�ĵ����ڿ����г��ȼ�գ����ò���ĵ���ʽΪ________��7.8g�ò�����������ˮ��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ____________________��
(4)z��e��f�ļ����Ӱ뾶�ɴ�С��˳��Ϊ_______________(�����ӷ��ű�ʾ)��
(5)��˵��g�ķǽ����Ա�fǿ��ʵ����ʵ��________________(�о�һ��)��
���𰸡� �ڶ����ڣ����2���ڣ� �ڢ�A�� ���Ӽ������ۼ������Լ����Թ��ۼ��� ![]() 0.1NA��6.02��1022 S2����O2����Al3�� HCl���ȶ��Ա�H2Sǿ��HClO4�����Ա�H2SO4ǿ��S2���Ļ�ԭ�Ա�Cl��ǿ��Cl2ͨ��Na2S��H2S��Һ�У���Һ�����
0.1NA��6.02��1022 S2����O2����Al3�� HCl���ȶ��Ա�H2Sǿ��HClO4�����Ա�H2SO4ǿ��S2���Ļ�ԭ�Ա�Cl��ǿ��Cl2ͨ��Na2S��H2S��Һ�У���Һ�����
����������ͼ�еĻ��ϼۡ�ԭ�Ӱ뾶�Ĵ�С��ԭ������,����֪��x��CԪ��,y��NԪ��,z��OԪ��,d��NaԪ��,e��AlԪ��,f��SԪ��,g��ClԪ����
(1)x��CԪ������2�����Ӳ�������������Ϊ4��λ�ڵ�2���ڵڢ�A����
��ˣ�������ȷ��������2���ڵڢ�A����
(2) N������������Ӧ��ˮ����HNO3�����⻯��NH3��Ӧ����NH4NO3��NH4NO3�к��л�ѧ��������Ϊ���Ӽ������ۼ���
��ˣ�������ȷ���������Ӽ������ۼ���
(3)Na�ĵ����ڿ����г��ȼ������Na2O2�������ʽΪ![]() ��
��
7.8 g Na2O2�����ʵ���Ϊ![]() =0.1mol�����ݷ�Ӧ����ʽ��2Na2O2+2H2O=4NaOH+O2����֪��1mol Na2O2��ˮ��Ӧת��1mol���ӣ���0.1mol Na2O2��������ˮ��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ0.1NA��6.02��1022 ��
=0.1mol�����ݷ�Ӧ����ʽ��2Na2O2+2H2O=4NaOH+O2����֪��1mol Na2O2��ˮ��Ӧת��1mol���ӣ���0.1mol Na2O2��������ˮ��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ0.1NA��6.02��1022 ��
��ˣ�������ȷ������![]() ��0.1NA��6.02��1022��
��0.1NA��6.02��1022��
(4)���Ӳ�ṹ��ͬ���������˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��O2����Al3����O2����Al3��2�����Ӳ�����S2��3�����Ӳ�������S2���뾶�����
��ˣ�������ȷ������S2����O2����Al3����
(5)Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ�������������ˮ��������Խǿ��������˵��Cl�ķǽ����Ա�Sǿ��ʵ����ʵ��HCl���ȶ��Ա�H2Sǿ��HClO4�����Ա�H2SO4ǿ��S2���Ļ�ԭ�Ա�Cl��ǿ��Cl2ͨ��Na2S��H2S����Һ�У���Һ�������
��ˣ�������ȷ������HCl���ȶ��Ա�H2Sǿ��HClO4�����Ա�H2SO4ǿ��S2���Ļ�ԭ�Ա�Cl��ǿ��Cl2ͨ��Na2S��H2S����Һ�У���Һ�������

����Ŀ����þ����һ�ֹ�ҵ���ϣ���Ҫ�ɷ���MgO(MgOռ40%,����CaO��MnO��Fe2O3��FeO��Al2O3��SiO2������)���Դ�Ϊԭ����ȡ������þ��������ӡȾ����ֽ��ҽҩ�ȹ�ҵ������þ������ȡMgSO4��7H2O����������:
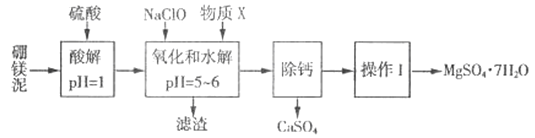
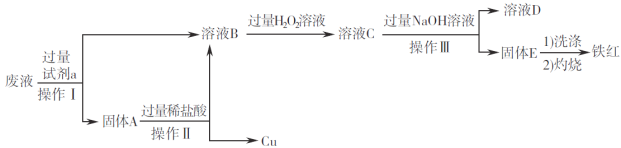
��������ش���������:
(1)ʵ��������1mol/L������800 mL������18.4 mol/L��Ũ���������ƣ�����ȡŨ����ʱ����ʹ�õ���Ͳ���Ϊ_______��(����ĸ)
A.10 mL B.25 mL C.50 mL D.100 mL
(2)�����NaClO �������Һ��Mn2+ ��Ӧ:Mn2+ + ClO-+H2O= MnO2 ��+ 2H+ + Cl-����Һ�л���һ������Ҳ�ᱻNaClO�������÷�Ӧ�����ӷ���ʽΪ___________���ò�����,����X��________(�ѧʽ)��
(3)���������г�MnO2��CaSO4 ���_______��(�ѧʽ)
(4)��֪MgSO4��CaSO4���ܽ�����±�:
�¶�/�� | 40 | 50 | 60 | 70 | |
�ܽ��/g | MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 | |
�����ơ��ǽ�MgSO4��CaSO4�����Һ�е�CaSO4��ȥ,�����ϱ�����,��Ҫ˵����������:____________��
(5)������I���ǽ���Һ����һϵ�в�������ո�����á���ո����ԭ����________��
(6)ʵ�����ṩ����þ�100g���õ���MgSO4��7H2O Ϊ147.6 g����MgSO4��7H2O�IJ���Ϊ________%��