题目内容
用如图所示装置可以完成一系列实验(图中夹持装置已略去)
请回答下列问题:
Ⅰ若气体a是Cl2,装置A、B、C中的试剂依次为:FeCl2溶液、淀粉KI溶液、石蕊溶液.
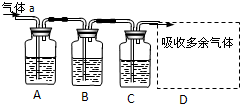
II若气体a是SO2,装置A、B、C中的试剂依次为:品红溶液、酸性高锰酸钾溶液、氢硫酸(硫化氢的水溶液).
(1)写出C中发生反应的化学方程式______.
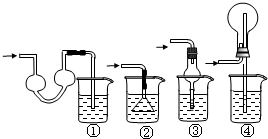
(2)D装置中用氢氧化钠溶液来吸收SO2,为了防止倒吸,应该选用下列装置中的______(填序号).
请回答下列问题:
Ⅰ若气体a是Cl2,装置A、B、C中的试剂依次为:FeCl2溶液、淀粉KI溶液、石蕊溶液.

| 装置 | A | B | C | D |
| 试剂 | FeCl2溶液 | 淀粉KI溶液 | 石蕊溶液 | ______ |
| 现象 | 溶液由浅绿色变为棕黄色 | ______ | ______ | |
| 离子方程式 | ______ | ______ | ______ |
| 装置 | A | B | C |
| 试剂 | 品红溶液 | 酸性高锰酸钾溶液 | 硫化氢的水溶液 |
| 现象 | ______ | 紫色褪去 | ______ |
| 体现SO2的性质 | ______ | ______ | 氧化性 |
(2)D装置中用氢氧化钠溶液来吸收SO2,为了防止倒吸,应该选用下列装置中的______(填序号).

Ⅰ若气体a是Cl2,装置A、B、C中的试剂依次为:FeCl2溶液、淀粉KI溶液、石蕊溶液,
氯气与A中氯化亚铁反应生成氯化铁,观察到溶液由浅绿色变为黄色,发生的离子反应为Cl2+2Fe2+=2Fe3++2Cl-,
与B中淀粉KI反应生成碘单质,观察到溶液变蓝,发生的离子反应为Cl2+2I-=I2+2Cl-,
与C中紫色石蕊试液先变红后褪色,D为尾气处理装置,与D中NaOH反应生成NaCl、NaClO和水,离子反应为Cl2+2OH-=Cl-+ClO-+2H2O,故答案为:
II若气体a是SO2,装置A、B、C中的试剂依次为:品红溶液、酸性高锰酸钾溶液、氢硫酸(硫化氢的水溶液),
二氧化硫使A中品红褪色,体现二氧化硫具有漂白性,与B中高锰酸钾发生氧化还原反应,体现其还原性,与C中硫化氢的水溶液发生氧化还原反应生成硫和水,观察到产生淡黄色沉淀,体现其氧化性,故答案为:
(1)C中二氧化硫与硫化氢反应生成硫和水,该反应为SO2+2H2S═3S↓+2H2O,故答案为:SO2+2H2S═3S↓+2H2O;
(2)所给的装置不会出现内外压强差,就能防止倒吸,图中①③具有缓冲的球形结构,不会形成压强差,则能起防倒吸的作用,故答案为:①③.
氯气与A中氯化亚铁反应生成氯化铁,观察到溶液由浅绿色变为黄色,发生的离子反应为Cl2+2Fe2+=2Fe3++2Cl-,
与B中淀粉KI反应生成碘单质,观察到溶液变蓝,发生的离子反应为Cl2+2I-=I2+2Cl-,
与C中紫色石蕊试液先变红后褪色,D为尾气处理装置,与D中NaOH反应生成NaCl、NaClO和水,离子反应为Cl2+2OH-=Cl-+ClO-+2H2O,故答案为:
| 装置 | A | B | C | D |
| 试剂 | NaOH溶液 | |||
| 现象 | 溶液变蓝 | 先变红后褪色 | ||
| 离子方程式 | Cl2+2Fe2+=2Fe3++2Cl- | Cl2+2I-=I2+2Cl- | Cl2+2OH-=Cl-+ClO-+2H2O |
二氧化硫使A中品红褪色,体现二氧化硫具有漂白性,与B中高锰酸钾发生氧化还原反应,体现其还原性,与C中硫化氢的水溶液发生氧化还原反应生成硫和水,观察到产生淡黄色沉淀,体现其氧化性,故答案为:
| 装置 | A | B | C |
| 试剂 | |||
| 现象 | 红色褪去 | 生成淡黄色沉淀 | |
| 体现SO2的性质 | 漂白性 | 还原性 |
(2)所给的装置不会出现内外压强差,就能防止倒吸,图中①③具有缓冲的球形结构,不会形成压强差,则能起防倒吸的作用,故答案为:①③.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目