题目内容
在下列叙述中,不能说明盐酸是强酸,醋酸是弱酸的是
| A.将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量多 |
| B.氯化钠溶液呈中性,醋酸钠溶液呈碱性 |
| C.相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
| D.等体积、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大 |
C
试题分析:弱电解质的证明,是基于与强电解质对比进行的。弱电解质与强电解质最大的区别就 是弱电解质存在电离平衡,而强电解质不存在电离平衡。因此只要证明有电离平衡存在, 就证明了弱电解质。A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量多,这说明在稀释过程中醋酸溶液中氢离子的物质的量是增加的,因此醋酸溶液中中存在电离平衡,可以说明盐酸是强酸,醋酸是弱酸;B、氯化钠溶液呈中性,醋酸钠溶液呈碱性,这说明氯离子不水解,CH3COO-水解,所以可以说明盐酸是强酸,醋酸是弱酸;C、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等,这说明由于起始时溶液中氢离子的浓度相同,因此不能盐酸是强酸,醋酸是弱酸;D、等体积、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大,说明增大CH3COO-的浓度抑制了醋酸的电离,说明可以说明盐酸是强酸,醋酸是弱酸,因此答案选C。

练习册系列答案
相关题目
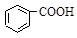 >HSO3->
>HSO3->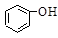 水杨酸(
水杨酸(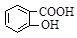 )与亚硫酸钠溶液反应,可能发生反应的离子方程式书写正确的是
)与亚硫酸钠溶液反应,可能发生反应的离子方程式书写正确的是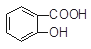 + SO32―→
+ SO32―→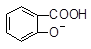 + HSO3―
+ HSO3―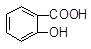 + SO32―→
+ SO32―→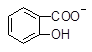 +HSO3―
+HSO3―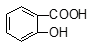 + SO32―→2
+ SO32―→2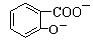 +2HSO3―
+2HSO3―
 CH3COO-+H+,要使电离平衡右移且c(CH3COO—)增大,应采取的措施是 ( )
CH3COO-+H+,要使电离平衡右移且c(CH3COO—)增大,应采取的措施是 ( )