题目内容
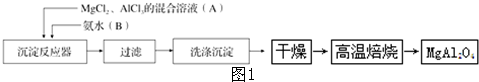
19.人工固氮是指将氮元素由游离态转化为化合态的过程.Ⅰ.最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实验氮的固定-一电解法合成氨,大大提高了氮气和氢气的转化率.
总反应式为N2+3H2$?_{一定条件下}^{SCT陶瓷}$2NH3.则在电解法合成氨的过程中,应将H2不断地通入阳极(填“阴”或“阳”);向另一电极通入N2,该电极的反应式为N2+6H++6e-=2NH3.
Ⅱ.据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3.相应的反应方程式为:2N2(g)+6H2O(g)?4NH3(g)+3O2(g)△H=Q
(1)上述反应的平衡常数表达式为$\frac{{c}^{4}(N{H}_{3})×{c}^{3}({O}_{2})}{{c}^{2}({N}_{2})×{c}^{2}({H}_{2}O)}$.
(2)取五份等体积N2和H2O的混合气体(物质的量之比均为1:3),分别加入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,反应相同时间后,测得氮气的体积分数φ(N2)与反应温度T的关系曲线如图1所示,则上述反应的Q>0(填“>”、“<”或“=”).
(3)若上述反应在有催化剂的情况下发生,则图2所示的a、b、c、d四条曲线中,能表示反应体系能量变化的是d(填字母代号),图中△H绝对值为1530kJ•mol-1.

Ⅲ.在一定温度下,将1molN2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
(1)达平衡时,H2的转化率a1=60%.
(2)在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为a2,当a1+a2=1时,则起始时NH3的物质的量n(NH3)=2mol.
分析 Ⅰ.在电解法合成氨的过程中,氢气发生氧化反应,应在阳极通入,氮气发生还原反应,在阴极通入,阴极上是氮获得电子,与质子结合生成氨气;
Ⅱ.(1)平衡常数为生成物平衡浓度化学计量数幂乘积与反应物平衡浓度化学计量数幂乘积的比;
(2)开始为到达平衡,氮气体积分数最大时到达平衡状态,而后升高温度,氮气的体积分数减小,说明升高温度平衡正向移动,则正反应为吸热反应;
(3)正反应为吸热反应,则反应物总能量小于生成物总能量,使用催化剂降低活化能,而反应热只与始态、终态有关,催化剂不影响反应热;
Ⅲ.(1)在一定温度下,将1molN2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol,设参加反应的氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):1 3 0
变化量(mol):x 3x 2x
平衡量(mol):1-x 3-3x 2x
再根据平衡时总物质的量列方程计算解答;
(2)在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为a2,当a1+a2=1时,则与原平衡为等效平衡,完全转化到左边满足1molN2和3mol H2.
解答 解:Ⅰ.在电解法合成氨的过程中,氢气发生氧化反应,应在阳极通入,氮气发生还原反应,在阴极通入,阴极上是氮获得电子,与质子结合生成氨气,阴极电极反应式为:N2+6H++6e-=2NH3,
故答案为:阳;N2+6H++6e-=2NH3;
Ⅱ.(1)2N2(g)+6H2O(g)?4NH3(g)+3O2(g)的平衡常数表达式K=$\frac{{c}^{4}(N{H}_{3})×{c}^{3}({O}_{2})}{{c}^{2}({N}_{2})×{c}^{2}({H}_{2}O)}$,
故答案为:$\frac{{c}^{4}(N{H}_{3})×{c}^{3}({O}_{2})}{{c}^{2}({N}_{2})×{c}^{2}({H}_{2}O)}$;
(2)开始为到达平衡,氮气体积分数最大时到达平衡状态,而后升高温度,氮气的体积分数减小,说明升高温度平衡正向移动,则正反应为吸热反应,则△H>0,
故答案为:>;
(3)正反应为吸热反应,则反应物总能量小于生成物总能量,使用催化剂降低活化能,而反应热只与始态、终态有关,催化剂不影响反应热,图中曲线d符合,
故答案为:d;
Ⅲ.(1)在一定温度下,将1molN2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol,设参加反应的氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):1 3 0
变化量(mol):x 3x 2x
平衡量(mol):1-x 3-3x 2x
故1-x+3-3x+2x=2.8,解得x=0.6,故氢气的转化率为$\frac{1.8mol}{3mol}$×100%=60%,
故答案为:60%;
(2)在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为a2,当a1+a2=1时,则与原平衡为等效平衡,完全转化到左边满足1molN2和3mol H2,则n(NH3)=2mol,
故答案为:2.
点评 本题考查化学平衡计算与影响因素、电解原理应用、等效平衡等,Ⅲ中(2)注意理解等效平衡规律,难度中等.

 阅读快车系列答案
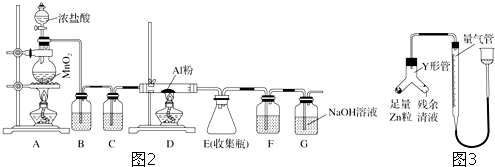
阅读快车系列答案 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH $→_{H_{2}SO_{4}加热}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/0C | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0g.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水放出大量热,容易发生迸溅伤人.
(2)加入沸石的作用是防止暴沸
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)分液漏斗使用前必须进行的操作是c(填正确答案标号).
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在下层(填“上”或“下”)
(6)反应温度应保持在90-95℃,其原因是:保证正丁醛及时蒸出,促使反应正向进行,又可尽量避免其被进一步氧化
(7)本实验中,正丁醛的产率为51%
(8)已知正丁醛在碱性条件下可以被新制氢氧化铜氧化,写出该反应的化学方程式:CH3CH2CH2CHO+NaOH+2Cu(OH)2$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.
| A. | ①中水的电离程度最小,③中水的电离程度最大 | |
| B. | 将②、③混合,若pH=7,则消耗溶液的体积②=③ | |
| C. | 将四份溶液稀释相同的倍数后,溶液的pH:③>④>②>① | |
| D. | 将①、④混合,若有c(CH3COO-)>c(H+),则混合溶液一定呈碱性 |
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
(1)在烧瓶中混合有机物及浓硫酸的方法是先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸,试管中盛放的液体可能是Na2CO3溶液,烧瓶中反应的方程式
 ,要想提高苯甲酸的转化率,可以采取的措施是加入过量的甲醇、移去苯甲酸甲酯
,要想提高苯甲酸的转化率,可以采取的措施是加入过量的甲醇、移去苯甲酸甲酯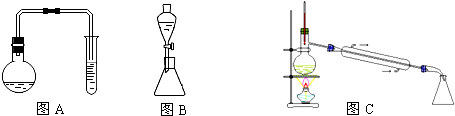
实验二:提纯苯甲酸甲酯
(2)停止加热,待烧瓶内的混合物冷却后,将试管及烧瓶中的液体转移到分液漏斗中,然后塞上分液漏斗的塞子再振荡后静置后,取下塞子、打开活塞,使(填主要成分的名称)苯甲酸甲酯进入锥形瓶,此时目标产物中所含杂质最多的物质是甲醇.
(3)用图C装置进行蒸馏提纯时,当温度计显示199.6 0C 时,可用锥形瓶收集苯甲酸甲酯.
实验三:探究浓硫酸在合成苯甲酸甲酯中的作用
(4)为确定浓硫酸对此反应存在催化作用,可另取等量反应物在不加浓硫酸情况下进行相同程度的加热,然后测量两个实验中的某种数据,该数据是相同时间内两个试管里生成有机层的厚度或两个试管中生成相同厚度的有机层所需的时间.
| A. | 使用催化剂可增大该反应速率 | |
| B. | 增大O2的浓度能加快反应速率 | |
| C. | 该反应达到平衡时,正、逆反应速率相等但不为0 | |
| D. | 一定条件下,2 mol SO2和1 mol O2反应可以得到2 mol SO3 |