��Ŀ����
��10�֣�������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�������������Ҫ�������£�
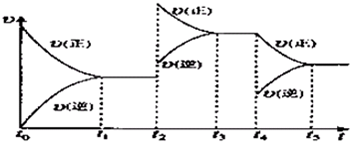
��1����N2��H2Ϊԭ�Ϻϳɰ�����һ���¶��£����ܱ������г���ImolN2��3molH2������Ӧ���������ݻ��㶨���ﵽƽ��״̬ʱ������������ʵ�����ԭ����![]() ����N2��ת����
����N2��ת����![]() ��������ѹǿ�㶨���ﵽƽ��״̬ʱ��N=��ת����Ϊ
��������ѹǿ�㶨���ﵽƽ��״̬ʱ��N=��ת����Ϊ![]() ����
����![]()
![]() �����>������<����=������
�����>������<����=������
��2���ð������������������ᣬ���������̿ɱ�ʾΪ��
4NH3+5O24NO+6H2O 4NO+3O2+2H2O=4HNO3
����3.4��Һ��Ϊԭ����������������Ϊ50%�����ᣬ��������Ҫ��ˮ������Ϊ
�֡����������������з�Ӧ��������������ģ�
��3�����Ṥҵ�����е�β�����ô�����Һ���գ��йصĻ�ѧ��ӦΪ��
2NO2+Na2CO3=NaNO2+NaNO3+CO2,NO+NO2+Na2CO3=2NaNO2+CO2�����ڱ�״������NO��NO2�Ļ�����壨������N2O4��ǡ����50mL 1�� 0 mol��L-1��Na2CO3��Һ��Ӧ��ȫ��������NaNO2��NaNO3�����ʵ����ı�Ϊ4��1�����ڻ��������NO������������Ϊ����?����д��������̣�
��1��12��5����1��8��>��4�֣�ÿ��2�֣� ��2��9��3�֣�
��2���������ɷ�Ӧ4NH3+5O24NO+6H2O��4NO+3O2+2H2O=4HNO3�ã�
NH3+2O2=HNO3+H2O��3.4��Һ������������Ϊ12.6�֣�ˮΪ3.6�֣������������ˮ������ ΪΪ��126.t/50%-(12.6+3.6)t=9t
��3����3�֣��ɷ�Ӧת����ϵ֪����Ӧ��������Ԫ���غ㣬��NaNO2��NaNO3�����ʵ����ֱ�Ϊ4a mol��a mol����4a+a=50mL��10-3mL��L-1��1��0 mol��L-1��2����ã�a=0��02 mol�����ǣ��Ƴ�NO��NO2�����ʵ�������Ϊ��0��03 mol��0��07 mol������NO��ռ���������Ϊ30����
����:

 ����������ϵ�д�
����������ϵ�д�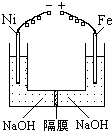 ��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��
��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g�� FeO��s��+CO��g������H��0
FeO��s��+CO��g������H��0