题目内容
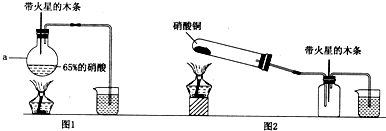
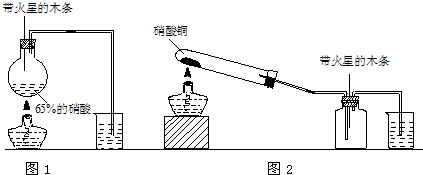
某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如图Ⅰ所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化碳和氧气。写出该反应的化学方程式:___________________________。
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确?_______(填“正确”或“不正确”),理由是___________________。
Ⅱ.实验装置如图Ⅱ所示
(1)写出浓硝酸受热分解的化学方程式:__________________________。
(2)实验开始后木条上的火星逐渐熄灭,有的同学提出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是______________________。
Ⅲ.为了更能直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。
(1)2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
(2)正确 硝酸铜分解产生的混合气体中氧气的体积分数与空气中氧气体积分数相当;空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧
Ⅱ.(1)4HNO3![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
(2)不正确 带火星的木条熄灭可能是由于加热时产生大量水蒸气所致
Ⅲ.用金属铜与浓HNO3反应制取NO2气体并用浓硫酸干燥,再将带火星木条伸入NO2中观察现象。
解析:2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑,由于硝酸铜分解产生的混合气体中氧气的体积分数与空气中氧气体积分数相当,空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。4HNO3==4NO2↑+O2↑+2H2O,由于加热时产生大量水蒸气所以带火星的木条熄灭。用金属铜与浓HNO3反应制取NO2气体并用浓硫酸干燥,再将带火星木条伸入NO2中。
2CuO+4NO2↑+O2↑,由于硝酸铜分解产生的混合气体中氧气的体积分数与空气中氧气体积分数相当,空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。4HNO3==4NO2↑+O2↑+2H2O,由于加热时产生大量水蒸气所以带火星的木条熄灭。用金属铜与浓HNO3反应制取NO2气体并用浓硫酸干燥,再将带火星木条伸入NO2中。

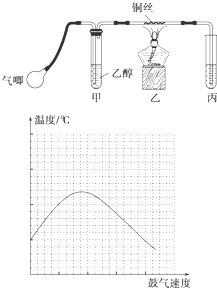 某研究性学习小组的同学利用如图所示装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.
某研究性学习小组的同学利用如图所示装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.