��Ŀ����
����Ŀ����ͼ��ʵ���ҳ��õ�װ�ã������Ҫ��ش����⣺
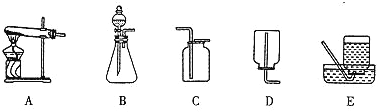
��1��ʵ����������غͶ���������ȡ�����Ļ�ѧ����ʽΪ________________________��ѡ�õ����巢��װ����_________����װ����ţ�����Ӧ��������Ҫ���˷�����������̣����˲������⣬����Ҫ����IJ�������������__________��__________��
��2��ʵ���ҿ��������ƹ�����Ũ��ˮ�ڳ����»����ȡ������NH3)��ѡ�õ����巢��װ����________����װ����ţ���
��3����ͼ�е�C��D��E����װ�ã���������ͼ��Fװ�ô��档����Fװ�ý����ſ������ռ�������̼��������̼Ӧ��Fװ�õ�_______���a����b������ͬ����ͨ�룻����Fװ�ý�����ˮ���ռ�������������Fװ����װ��ˮ��Ȼ��������Fװ�õ�_______��ͨ�롣
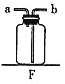
��4����������̼ͨ����ɫʯ����Һ�У���Һ��ɺ�ɫ�����Ⱥ���Һ�ֱ����ɫ���û�ѧ����ʽ��ʾ���Ⱥ���Һ�ֱ����ɫ��ԭ����_____________________��
���𰸡�2KClO3![]() 2KCl+3O2�� A�ձ�©��B baH2CO3
2KCl+3O2�� A�ձ�©��B baH2CO3![]() H2O+CO2��
H2O+CO2��
��������
��1��ʵ����������غͶ���������ȡ�����Ļ�ѧ����ʽΪ2KClO3![]() 2KCl+3O2�����÷�Ӧ���ڹ������������Ʊ�����ķ�Ӧ�����ѡ�õ����巢��װ����A���������̲�����ˮ����Ӧ��������Ҫ���˷�����������̣����˲������⣬����Ҫ����IJ��������������ձ���©����
2KCl+3O2�����÷�Ӧ���ڹ������������Ʊ�����ķ�Ӧ�����ѡ�õ����巢��װ����A���������̲�����ˮ����Ӧ��������Ҫ���˷�����������̣����˲������⣬����Ҫ����IJ��������������ձ���©����
��2��ʵ���ҿ��������ƹ�����Ũ��ˮ�ڳ����»����ȡ������NH3)���÷�Ӧ���ڹ�����Һ�巴Ӧ����Ҫ�����Ʊ�����ķ�Ӧ��ѡ�õ����巢��װ����B��
��3��������̼�ܶȴ��ڿ�������Ҫ�����ſ������ռ�������Fװ�ý����ſ������ռ�������̼��������̼Ӧ��Fװ�õ�b��ͨ�룻����Fװ�ý�����ˮ���ռ�������ˮ��b���ų����������Fװ����װ��ˮ��Ȼ��������Fװ�õ�a��ͨ�롣
��4����������̼ͨ����ɫʯ����Һ�У�������̼��ˮ��Ӧ����̼�ᣬ��Һ�����ԣ���Һ��ɺ�ɫ�����Ⱥ�̼��ֽ⣬�����Һ�ֱ����ɫ����Ӧ�Ļ�ѧ����ʽΪH2CO3![]() H2O+CO2����
H2O+CO2����

 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�����Ŀ������ 4��ͼ������ȷ��ӳ��Ӧ�仯��ϵ�ǣ� ��
A | B | C | D |
|
|
|
|
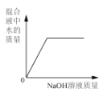
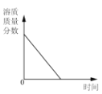
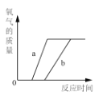
��һ����ϡ�����м��� NaOH ��Һ | Ũ���᳤�ڱ�¶�ڿ����� | ��һ������������Һ����ε�������������Һ������ | ��ͬ�����£����ȵ����������ݹ��壬aΪ����غͶ������̵Ļ���b Ϊ����� |
A. A B. B C. C D. D
����Ŀ���״�����Ϊȼ�ϵ�ص�ԭ�ϡ���ҵ������CO2��H2��һ�������·�Ӧ�ϳɼ״���
��1����֪�ڳ��³�ѹ����
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H����1275.6 kJ��mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H����566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H����44.0 kJ��mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��2���״��������ȡ��ȩCH3OH(g)![]() HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯��������ͼ��ʾ���ش��������⣺
HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯��������ͼ��ʾ���ش��������⣺

��600Kʱ��Y��״��Ħ�(��) (��)���>����<����
�ڴ�Y�㵽X��ɲ�ȡ�Ĵ�ʩ��____________________________��
����ͬѧ����õ���t1Kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ8.1mol��L��1������Ϊ��ȷ����˵������ ��
��3������Cu2O���ھ��������Ĵ����ܶ��ܵ���ע������ͬ���ܱ������У�ʹ�ò�ͬ�����Ƶõ�Cu2O���ͣ��ֱ���д�CH3OH������ʵ�飺CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH��Ũ�ȣ�mol��L��1����ʱ��t (min)�仯���±���
��� | �¶� | 0 | 10 | 20 | 30 | 40 | 50 |
�� | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
�� | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
�� | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
�����жϣ�ʵ��ٵ�ǰ20 min��ƽ����Ӧ���� ��(H2)�� ��ʵ���¶�T1 T2���>������<�����������Ĵ�Ч�ʣ�ʵ��� ʵ��ڣ��>������<������
��4����ⷨ�������״���ˮ����ɵ���Ⱦ��ԭ���ǣ�ͨ�罫Co2+������Co3+��Ȼ��Co3+���״�������CO2��H+����ʯīϩ������ȥCo2+������������ͼ��ʾװ��ģ���������̣� ��ȥ�״������ӷ���ʽΪ ��