题目内容
a、b、c、d是四种短周期的主族元素.a、b、d同周期,其中d的质子数最大;a、c同主族.a的原子结构示意图为: ;a与b形成化合物的电子式为:
;a与b形成化合物的电子式为: .
.
下列叙述正确的是( )
 ;a与b形成化合物的电子式为:
;a与b形成化合物的电子式为: .
.下列叙述正确的是( )
分析:a、b、c、d是四种短周期的主族元素.a的原子结构示意图为: ,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为:
,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为: ,b形成+1价离子,故b为Na元素,根据元素所在周期表中的位置结合元素周期律的递变性和相似性解答该题.
,b形成+1价离子,故b为Na元素,根据元素所在周期表中的位置结合元素周期律的递变性和相似性解答该题.
 ,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为:
,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为: ,b形成+1价离子,故b为Na元素,根据元素所在周期表中的位置结合元素周期律的递变性和相似性解答该题.
,b形成+1价离子,故b为Na元素,根据元素所在周期表中的位置结合元素周期律的递变性和相似性解答该题.解答:解:a、b、c、d是四种短周期的主族元素.a的原子结构示意图为: ,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为:
,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为: ,b形成+1价离子,故b为Na元素,
,b形成+1价离子,故b为Na元素,
A.同主族自上而下原子半径增大,同周期自左而右原子半径减小,故原子半径b>a>c,故A错误;
B.同主族自上而下非金属性减弱,同周期自左而右非金属性增强,故非金属性O>S,Cl>S,故B错误;
C.水中存在氢键,常温下为液体,氯化氢、硫化氢为气态,故水的沸点最高,氯化氢、硫化氢结构相似相对分子质量越大沸点越高,故沸点a>d>c,故C错误;
D.O与S可以形成二氧化硫、三氧化硫,O与Na能形成氧化钠、过氧化钠,故D正确;
故选D.
 ,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为:
,第一电子层容纳2个电子,故x=2,则a的质子数为16,故a为S元素;a、c同主族,则c为O元素;a、b、d同周期,其中d的质子数最大,则d为Cl元素;a与b形成化合物的电子式为: ,b形成+1价离子,故b为Na元素,
,b形成+1价离子,故b为Na元素,A.同主族自上而下原子半径增大,同周期自左而右原子半径减小,故原子半径b>a>c,故A错误;
B.同主族自上而下非金属性减弱,同周期自左而右非金属性增强,故非金属性O>S,Cl>S,故B错误;
C.水中存在氢键,常温下为液体,氯化氢、硫化氢为气态,故水的沸点最高,氯化氢、硫化氢结构相似相对分子质量越大沸点越高,故沸点a>d>c,故C错误;
D.O与S可以形成二氧化硫、三氧化硫,O与Na能形成氧化钠、过氧化钠,故D正确;
故选D.
点评:本题考查原子结构与元素周期律、常用化学用语等,难度不大,注意根据原子结构示意图与电子式推断元素.

练习册系列答案
相关题目
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为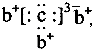 下列比较中正确的是( )
下列比较中正确的是( )
 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为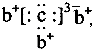 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
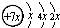 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
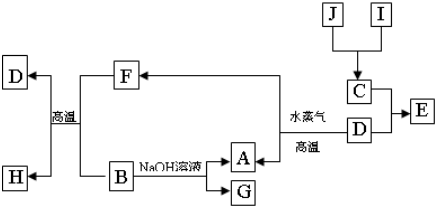
 Al(OH)3+OH-
Al(OH)3+OH-