题目内容
【题目】25℃下,弱电解质的电离平衡常数![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.用0.1mol/L的盐酸滴定0.1mol/L的氨水时,可用酚酞作指示剂
B.0.2mol/L的醋酸与0.1mol/L的氢氧化钠溶液等体积混合,所得溶液中:![]()
C.pH=3的盐酸与pH=11的氨水等体积混合,所得溶液中![]()
D.pH=3的醋酸与pH=11的氨水等体积混合,所得溶液中由水电离出的![]()
【答案】C
【解析】
A.选择指示剂:指示剂的变色范围应与反应后溶液溶质的pH吻合,反应后溶质为NH4Cl,溶液显酸性,因此选择甲基橙为指示剂,故A错误;
B.0.2 mol/L的醋酸与0.1 mol/L的氢氧化钠溶液等体积混合,得到等浓度的醋酸钠和醋酸混合溶液,溶液中电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+),物料守恒2c(Na+)=c(CH3COO-)+c(CH3COOH),得到c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+),故B错误;
C.NH3H2O是弱碱,HCl是强酸,因此pH=3的盐酸与pH=11的氨水:c(NH3H2O)>c(HCl),即反应后溶质为NH4Cl和NH3H2O,NH3H2O的物质的量浓度大于NH4Cl,NH3H2O的电离大于NH4+的水解,溶液显碱性,所得溶液中![]() ,故C正确;
,故C正确;
D.常温下,Ka(CH3COOH)=Kb(NH3H2O)=1.75×10-5,醋酸根离子和铵根离子都发生水解,二者水解程度相近,溶液pH=7,由于水解促进水的电离,所得溶液中由水电离出的c(H+)>1×10-7 mol/L,故D错误;
故答案选C。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】合理利用资源成为当今研究热点。CH3NH2、PbI2及HI常用作合成太阳能电池的敏化剂甲胺铅碘(CH3NH3PbI3)的主要原料。
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | E1 | E2 | E3 | E4 |
则上述热化学方程式中ΔH=___kJ·mol-1。
(2)可利用水煤气合成上述反应所需甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②图中Y轴表示温度,其判断的理由是__。
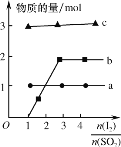
(3)可利用四氧化三铅和氢碘酸反应制备难溶PbI2,若反应中生成amolPbI2,则转移电子的物质的量为___。
(4)将二氧化硫通入碘水制备HI的反应曲线如图所示,其反应原理为:SO2+I2+2H2O=3H++HSO4-+2I-,I2+I-![]() I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
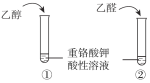
【题目】下列实验内容能达到实验目的的是
实验目的 | 实验内容 | |
A | 鉴别乙醇与乙醛 |
|
B | 比较乙酸、碳酸、苯酚的酸性 |
|
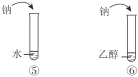
C | 说明烃基对羟基上氢原子活性的影响 | |
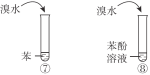
D | 说明苯环对取代基上氢原子活性的影响 |
|
A. AB. BC. CD. D