题目内容
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )
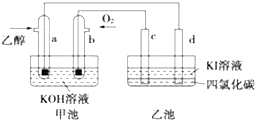

| A、两个装置之间没有盐桥,故不能形成电流 |
| B、a电极的电极反应式:C2H5OH+16OH--12e-═2CO32-+11H2O |
| C、一段时间后,乙池d电极周围的溶液呈现棕褐色 |
| D、乙池在反应前后溶液的pH不变 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:燃料电池中,通入燃料的电极是负极,负极上失电子发生氧化反应,在乙池中,乙池溶液分层,上层溶液为盐溶液,电解时阴极上氢离子放电同时生成氢氧根离子,电极反应中后碘单质生成,阳极上碘离子失电子发生氧化反应,以此解答该题.
解答:
解:A.图示是原电池与电解池的联合装置,不需要盐桥就能形成电流,故A错误;
B.乙醇作还原剂,失电子,电极方程式为C2H5OH+16OH--12e-═2CO32-+11H2O,发生氧化反应,故B正确;
C.乙池中,阳极反应式:2I--2e-═I2,c电极为阳极,生成单质碘,故c电极周围的溶液呈棕褐色,故C错误;
D.d电极作阴极,阴极反应式:2H2O+2e-═H2↑+2OH-,故乙池溶液的pH增大,故D错误,
故选B.
B.乙醇作还原剂,失电子,电极方程式为C2H5OH+16OH--12e-═2CO32-+11H2O,发生氧化反应,故B正确;
C.乙池中,阳极反应式:2I--2e-═I2,c电极为阳极,生成单质碘,故c电极周围的溶液呈棕褐色,故C错误;
D.d电极作阴极,阴极反应式:2H2O+2e-═H2↑+2OH-,故乙池溶液的pH增大,故D错误,
故选B.
点评:本题综合考查原电池和电解池知识,侧重于学生的分析能力和应用能力的考查,注意把握电极方程式的书写,为解答该题的关键,难度中等.

练习册系列答案
相关题目
下列化学反应的离子方程式,书写正确的是( )
| A、碳酸钙与稀盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氢氧化铁溶于盐酸:Fe(OH)3+3H+═Fe3++3H2O |
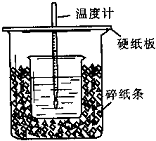 某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )
某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )| A、图中实验装置缺少环形玻璃搅拌棒 |
| B、烧杯间填满碎纸条的作用是固定小烧杯 |
| C、大小烧杯的杯口不相平,对实验结果无影响 |
| D、大烧杯上不盖硬纸板,求得的中和热△H会偏小 |
下列说法不正确的是( )
| A、室温下,44g乙醛和乙酸乙酯的混合物中含有的碳原子数目为2NA |
| B、标准状况下,22.4L甲醇中含有的氧原子数为1.0NA |
| C、食醋中含有乙酸,乙酸可由乙醇连续氧化得到 |
| D、煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 |
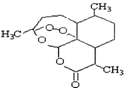 被誉为中国“新四人发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,
被誉为中国“新四人发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,主要成分是青蒿素,结构如图所示.有关该化合物的叙述正确的是( )
| A、分子式为C16H22O5 |
| B、该化合物不能与NaOH溶液反应 |
| C、该化合物中含有过氧键,在一定条件下有氧化性 |
| D、青蒿素易溶于水 |
下列化合物,依次属于氧化物、碱、盐的一组是( )
| A、Na2CO3、KOH、CaO |
| B、CO、NaOH、KCl |
| C、H2O、H2SO4、NaCl |
| D、CO2、KOH、FeO |
下列实验操作或对实验事实的描述正确的是( )
| A、中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒 |
| B、用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小 |
| C、测定硫酸铜晶体结晶水含量,若加热后的粉末表面发黑,则所测结晶水含量可能会偏高 |
| D、锌和一定量稀硫酸反应,为加快速率而不影响如的量可向溶液中加适量Cu(NO3)2晶体 |
已知428℃时,H2(g)+I2(g)?2HI(g)的平衡常数为49,则该温度下2HI(g)?H2(g)+I2(g)的平衡常数是( )
A、
| ||
B、
| ||
| C、492 | ||
| D、无法确定 |