题目内容
合成氨反应中,若进口时N2、H2、NH3的体积之比为5:15:3,出口时N2、H2、NH3的体积之比为9:27:8,则N2的转化率为( )
| A、10% | B、20% |
| C、30% | D、40% |
考点:化学平衡的计算
专题:化学平衡专题
分析:根据体积之比等于物质的量之比,则可设进口时N2、H2、NH3的物质的量分别为5a、15a、3a,出口时N2、H2、NH3的体积之比为9b、27b、8b,利用三段式,求得氮气转化了的物质的量,再根据转化率的定义可求得N2的转化率;
解答:
解:根据体积之比等于物质的量之比,则可设进口时N2、H2、NH3的物质的量分别为5a、15a、3a,出口时N2、H2、NH3的体积之比为9b、27b、8b,利用三段式,
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
初始量:5a 15a 3a
变化量:5a-9b 15a-27b 8b-3a
平衡量:9b 27b 8b
则有
=
,解得a=2b,所以N2的转化率为
×100%=
×100%=10%,故选A.
N2(g)+3H2(g)
 2NH3(g)
2NH3(g)初始量:5a 15a 3a
变化量:5a-9b 15a-27b 8b-3a
平衡量:9b 27b 8b
则有
| 5a-9b |
| 8b-3a |
| 1 |
| 2 |
| 5a-9b |
| 5a |
| 2×5b-9b |
| 5×2b |
点评:本题主要考查了根据化学方程式进行计算,难度不大,解题关键要抓住变化量之比等于计量数之比.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列粒子浓度关系不正确的是( )
| A、Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| B、NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、pH=2的盐酸与pH=12的氨水以任意比例混合所得溶液中:c(H+)+c(NH4+)=c(OH-)+c(Cl-) |
| D、等物质的量浓度的CH3COOH和CH3COONa溶液等体积混合后所得溶液中:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
下列化学反应的离子方程式,书写正确的是( )
| A、碳酸钙与稀盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氢氧化铁溶于盐酸:Fe(OH)3+3H+═Fe3++3H2O |
下列叙述正确的是( )
| A、NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1:2 |
| B、离子化合物中一定不含共价键 |
| C、某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H2m-nR |
| D、NaHSO4、Na2O2二者熔化时只破坏离子键,碘升华只需要克服分子间作用力 |
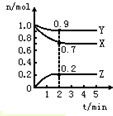 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,下列表述正确的是( )
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,下列表述正确的是( )| A、该反应的化学方程式为X+3Y═2Z |
| B、反应开始至2min,以气体Z表示的平均反应速率为0.1mol/(L?min) |
| C、在2min内,分别用X、Y、Z三种物质表示化学反应平均速率其比值为:1:3:2 |
| D、在2min后,若向该密闭容器中再加入催化剂,则各物质的浓度不会变化. |
下列有机物中,在一定条件下不能发生水解的是( )
| A、葡萄糖 | B、纤维素 |
| C、脂肪 | D、蛋白质 |
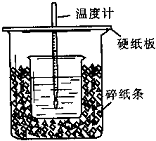 某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )
某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )| A、图中实验装置缺少环形玻璃搅拌棒 |
| B、烧杯间填满碎纸条的作用是固定小烧杯 |
| C、大小烧杯的杯口不相平,对实验结果无影响 |
| D、大烧杯上不盖硬纸板,求得的中和热△H会偏小 |
下列说法不正确的是( )
| A、室温下,44g乙醛和乙酸乙酯的混合物中含有的碳原子数目为2NA |
| B、标准状况下,22.4L甲醇中含有的氧原子数为1.0NA |
| C、食醋中含有乙酸,乙酸可由乙醇连续氧化得到 |
| D、煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 |
已知428℃时,H2(g)+I2(g)?2HI(g)的平衡常数为49,则该温度下2HI(g)?H2(g)+I2(g)的平衡常数是( )
A、
| ||
B、
| ||
| C、492 | ||
| D、无法确定 |