题目内容
实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g) 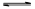 NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
(1)该反应在一定条件下能够自发进行,则反应的ΔH 0。(填大于、小于或等于)
(2)写出生成碳酸氢铵的化学方程式 。
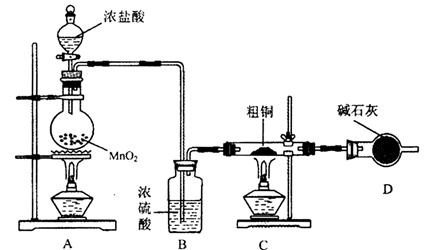
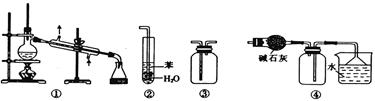
(3)按下图装置进行如下实验:
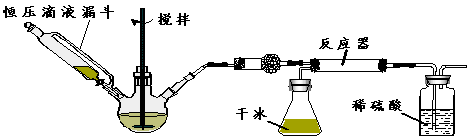
步骤1:检查装置气密性。
步骤2:在相应仪器中装入药品,其中在三颈烧瓶中加入足量的氢氧化钠固体,恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品
……
①干燥管中盛放的药品是 。
②对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有 。
③以恒压滴液漏斗代替分液漏斗的目的是 。
④反应后期随着CO2气流减慢,导致反应物比例不当,可采取的相应措施是 。
(4)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是 。
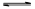 NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。(1)该反应在一定条件下能够自发进行,则反应的ΔH 0。(填大于、小于或等于)
(2)写出生成碳酸氢铵的化学方程式 。
(3)按下图装置进行如下实验:

步骤1:检查装置气密性。
步骤2:在相应仪器中装入药品,其中在三颈烧瓶中加入足量的氢氧化钠固体,恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品
……
①干燥管中盛放的药品是 。
②对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有 。
③以恒压滴液漏斗代替分液漏斗的目的是 。
④反应后期随着CO2气流减慢,导致反应物比例不当,可采取的相应措施是 。
(4)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是 。
(1)小于(2分)
(2)NH3+CO2+H2O=NH4HCO3(2分)
(3)①固体氢氧化钠或碱石灰(2分)
②不需要干燥;提供低温环境,提高转化率(2分 答对任意一点就给分)
③使氨水顺利滴下(2分) ④调节恒压滴液漏斗旋塞,减慢氨水滴加速度(2分)
(4)产品易堵塞导管,稀硫酸会倒吸(2分)
(2)NH3+CO2+H2O=NH4HCO3(2分)
(3)①固体氢氧化钠或碱石灰(2分)
②不需要干燥;提供低温环境,提高转化率(2分 答对任意一点就给分)
③使氨水顺利滴下(2分) ④调节恒压滴液漏斗旋塞,减慢氨水滴加速度(2分)
(4)产品易堵塞导管,稀硫酸会倒吸(2分)
试题分析:(1)根据方程式2NH3(g)+CO2(g)
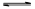 NH2COONH4(s)可知,该反应是熵值减小的可逆反应。如果该反应在一定条件下能够自发进行,则根据△G=△H-T·△S可知,该的焓变ΔH一定小于0。
NH2COONH4(s)可知,该反应是熵值减小的可逆反应。如果该反应在一定条件下能够自发进行,则根据△G=△H-T·△S可知,该的焓变ΔH一定小于0。(2)有水参加,则生成碳酸氢铵,因此反应的化学方程式为NH3+CO2+H2O=NH4HCO3。
(3)①由于制备氨基甲酸铵的原料氨气必须是干燥的,以防止副反应的发生,因此生成的氨气必须进行干燥。因为氨气是碱性气体,所以干燥氨气应该用固体氢氧化钠或碱石灰。
②碳酸盐和酸反应制CO2,则生成的CO2必须进行净化和干燥处理,而直接利用干冰制备CO2,不需要干燥;又因为该反应是放热反应,提供低温环境,可以提高转化率。
③恒压滴液漏斗代替分液漏斗可以平衡内外压强,使氨水顺利滴下。
④反应后期随着CO2气流减慢,导致反应物比例不当,此时可以通过调节恒压滴液漏斗旋塞,减慢氨水滴加速度加以控制。
(4)由于氨基甲酸铵是固体,所以产品易堵塞导管。又因为氨气极易溶于水,直接插入稀硫酸中吸收氨气,容易使稀硫酸倒吸。

练习册系列答案
相关题目
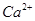 、
、 、
、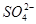 ,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是
,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是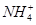
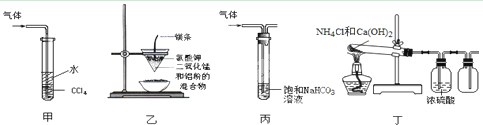
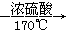 CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。